妈妈为小鹏准备了一份午餐:米饭、红烧肉、糖醋鱼、咸鸭蛋、豆腐汤、酸奶。请回答下列问题:
(1)为保证各种营养素的均衡摄入,午餐中还应补充的营养素是 。
(2)做红烧肉时,油锅起火,妈妈立即盖上锅盖。其灭火原理是 。
(3)午饭后,小鹏感到胃不舒服,服用含氢氧化铝的药物中和过多的胃酸,症状有所缓解。写出该反应的化学方程式 。
(4)废弃的酸奶袋等塑料垃圾会造成“白色污染”,请写出一条解决“白色污染”的措施 。
某研究性学习小组通过查阅资料获知以下信息:将二氧化碳气体慢慢地通入一定量的氢氧化钠溶液中,在溶液中先后发生以下两个化学反应:
2232O (先发生反应)
23223 (后发生反应)
同学们开展了下列探究活动:
【提出问题】将二氧化碳气体慢慢地通入一定量的氢氧化钠溶液中,反应后所得溶液中溶质的成分有哪些?
23;
23;
Ⅲ. ;
Ⅳ. .
【实验探究】将二氧化碳气体慢慢地通入一定量的某氢氧化钠溶液中,再将反应后所得溶液按下列流程进行实验并测出相关数据:

332易溶.
【获得结论】根据上述信息,分析反应后所得溶液中溶质的成分并计算溶质的质量,将结
果填入下表:
|
溶质的化学式 |
溶质的质量/g |
填表说明:①不写计算过程,计算结果保留一位小数.
②如果溶质的成分只有一种,请填写在第一行;如果溶质的成分有两种,请分别在两行中各填写一种物质.
某化工厂的废液中主要含有硝酸银、硝酸铜。取一定量的该废液样品,加入镁粉和铜粉,充分反应后过滤,得到滤液和滤渣。 请填写下列空格:
(1)若滤渣中有镁粉,则滤渣中除镁粉外还含有 (填写化学式,下同)。
(2)若滤渣中有铜粉,则滤液中的溶质一定含有 ,可能含有 。
(3)若滤渣中没有铜粉,则滤液中的溶质一定含有 ,可能含有 。
(4)反应后得到滤液的质量 (选填“小于”、“大于”或“等于”)反应前所取废液样品的质量。
实验室用100g 溶质质量分数为 6.8%的过氧化氢溶液与少量二氧化锰混合制取氧气,计算完全反应后生成氧气的质量是多少?(写出计算步骤,计算结果保留一位小数)
化学实验是进行科学探究的重要手段。请填写下列空格:
(1)黄铜是铜锌合金,将外形完全相同的纯铜片和黄铜片相互刻划,该实验的目的是比较它们的 大小。
(2)用坩埚钳夹取一小块木炭,在酒精灯上加热至燃烧,然后将木炭插入盛有氧气的集气瓶内,观察现象。 据此可知,可燃物燃烧的剧烈程度与 有关。
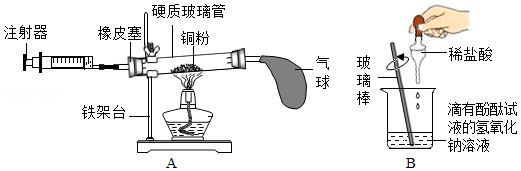
(3)用图 A 所示的装置可测定空气中氧气的含量。 该实验的原理是通过 (选填“化学”或“物理”)方法分离或除去混合物中的一种成分,从而测定混合物中某成分的含量。
(4)用图B 所示的装置探究酸碱中和反应。将稀盐酸滴入氢氧化钠溶液(滴有酚酞试液)中至过量,观察到的现象是 。从微观角度分析,中和反应的实质是 。 请另外写出一个符合上述反应实质的化学方程式 。
能源、材料、环保、食品等问题越来越引起人们的重视.请从化学的视角分析下列有关问题并填写空格:
(1)化石燃料包括煤、石油和 .
(2)铝合金可用于制造飞机的外壳,铝合金属于 (选填“合成材料”、“金属材料”或“复合材料”).
(3)塑料在为我们的生活创造便利的同时,也对环境造成不利影响. 人们把塑料给环境带来的危害称为“ ”.
(4)为了合理膳食,营养均衡,生活中把榨好的蔬菜汁放到面粉中,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养物质是 和 .
22]属于 (选填“氮肥”、“钾肥”或“磷肥”).