面粉是制作美食的原材料。在发面团的过程中会生成酸而影响口味,为使食品更美味,可以加碱面处理。碱面的主要成分为碳酸钠(Na2CO3),为测定某品牌碱面中碳酸钠的质量分数,小金按照如图甲所示实验装置,利用碱面与盐酸反应生成二氧化碳气体的质量来计算碱面中碳酸钠的质量分数(杂质不与盐酸反应)。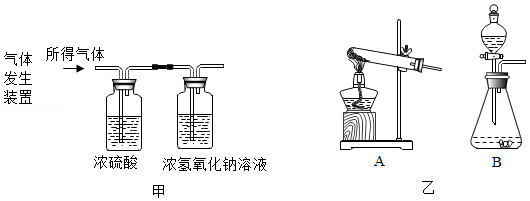
完成下列问题:
(1)为完成碳酸钠质量分数的测定实验,气体发生装置应选择图乙中的 装置(填字母)。
(2)小金各取11.0克碱面样品与一定量的稀盐酸进行三次实验,三次实验所采集的数据见表。合理选择表中数据并计算碱面中碳酸钠的质量分数;
实验次数 |
碱面样品质量/克 |
稀盐酸质量/克 |
二氧化碳质量/克 |
1 |
11.0 |
50.0 |
1.1 |
2 |
11.0 |
200.0 |
4.4 |
3 |
11.0 |
250.0 |
4.4 |
(3)按照图甲实验装置测定的CO2气体质量,可能导致CO2质量测定结果偏小的原因 (写出一种即可)。
某同学用质量分数为15%的稀硫酸处理某造纸厂含NaOH的碱性废水样品:
(1)用9.2g质量分数为98%的浓硫酸能配制上述稀硫酸 g(计算结果保留整数)。
(2)若上述造纸厂废水75g能与9.8g 15%的稀硫酸恰好反应(设只发生NaOH与硫酸的反应),试计算该废水中NaOH的质量分数(写出计算过程,结果精确到0.1%)。
某同学对碳酸钠、碳酸氢钠的组成及某些性质进行探究。
[认识组成](1)由化学式Na2CO3、NaHCO3可知,两者含有的元素差别是 ;从构成离子的层次看,酸根离子分别是CO32﹣、HCO3﹣,依据酸根离子它们都可统称为 (填“碳酸盐”或“钠盐”)。
[比较性质](2)为比较室温是20℃时Na2CO3、NaHCO3与水混合的变化,按图1进行实验,先向两支试管中分别加入各约1g Na2CO3、NaHCO3,再分别滴入几滴水,振荡后将温度计插入其中,发现盛有Na2CO3的试管中温度计的示数高于20℃,盛有NaHCO3的试管中温度计的示数低于20℃;再向两试管中各加入约5mL水和2滴酚酞试液,振荡后液体均呈红色。则NaHCO3与水混合时 (填“放出”或“吸收”)热量,NaHCO3溶液显 (填“酸性”或“碱性”)。
[提出问题](3)Na2CO3、NaHCO3还有什么不同性质?

[查阅资料]NaHCO3受热易分解生成Na2CO3、H2O和CO2.Na2CO3受热不易分解。可用图2装置验证。
[进行实验]按图2连接装置,检查气密性后,分别装入相关药品(试管甲、乙中的固体质量应相等)。后续实验均按规范要求进行,完成实验。
①若要使实验效果更理想,则甲中应装入 (填“Na2CO3”或“NaHCO3”)。
②完成实验后,待试管冷却至室温,若甲、乙试管里剩余固体的质量分别用m(甲)、m(乙)表示,则m(甲) (填“>”或“=”或“<”)m(乙)。
[拓展应用](4)若把碳酸和NaHCO3比较,受热容易分解的是 (填“碳酸”或“NaHCO3”)。除去Na2CO3粉末中混有的少量NaHCO3的方法是 。
(5)研究表明,Na2CO3在水中溶解时能生成自由移动的离子,且Na2CO3溶液中还含有很少的HCO3﹣,在Na2CO3溶液中存在的带负电荷的离子有HCO3﹣、 、 (填离子符号)。
请根据如图1实验装置图回答问题:

(1)实验室制取二氧化碳的发生装置是 (填字母),反应的化学方程式为 。
(2)实验室用装置A加热高锰酸钾制取氧气的化学方程式为 ,在试管口放置蓬松的棉花团的目的是 。用排空气法收集氧气时,检验是否收集满的操作方法是 。
(3)已知:通常状况下,二氧化硫气体的密度比空气大,易溶于水,能与水反应生成亚硫酸。实验室常用亚硫酸钠与硫酸在常温下反应制取SO2。
①实验室制取SO2的发生装置可用 (填字母),收集SO2的装置可用 (填字母)。
② 如图2所示,把充满SO2的试管倒立在滴有紫色石蕊的水中,可看到的现象是试管内 且液体变为红色,其中液体变为红色的原因是液体中产生了 (填物质的化学式)。
CO2是最主要的温室气体,也是巨大的碳资源,CO2的低能耗捕集、转化和利用正受到世界各国的广泛关注。

(1)以CO2为原料制取炭黑的太阳能工艺如图1所示。
①反应1的基本类型为 。
②反应2中碳元素的化合价 (填“升高”“不变”或“降低”)。
(2)利用NaOH溶液吸收CO2,部分转化关系见图2。
反应①的化学方程式为 ,该转化中循环使用的物质是 。
(3)利用Na2CO3或K2CO3溶液吸收低浓度的CO2,将其转化为NaHCO3或KHCO3,NaHCO3或KHCO3受热分解生成高浓度的CO2储存利用,生成的Na2CO3或K2CO3循环使用以降低生产成本。
|
吸收剂 |
Na2CO3 |
K2CO3 |
|
20℃最高浓度(g/L) |
212 |
1104 |
|
价格(元/Kg) |
1.25 |
9.80 |
根据表中信息,选择K2CO3溶液作吸收液的优点是 。
(4)利用一种新型“人造树叶”将CO2转化为乙醇(C2H5OH)的反应如下:2CO2+3H2O C2H5OH+3O2,研究显示,1L“人造树叶”每天能从空气中吸收968g CO2,计算1L“人造树叶”工作1天可得到乙醇的质量(写出计算过程)。
(5)某研究小组设计如图3所示实验,探究CO2和H2在一定条件下反应的产物。
查阅资料:①CO2和H2在合适催化剂和一定温度下反应转化为CO和H2O;
②白色无水硫酸铜吸水后变为蓝色。

实验过程中观察到的主要现象有:B装置中白色固体变为蓝色,C装置中黑色固体变为红色,D装置中澄清石灰水变浑浊。
①设计B装置的目的是 。
②C装置中发生的反应的化学方程式为 。
③研究小组反思后认为,根据上述实验现象不能确认CO2和H2反应生成了CO,理由是 。
硼及其化合物在现代工农业、医学、国防中有着重要的应用价值。利用硼镁矿可制备硼,工艺流程如图所示。请回答下列问题:
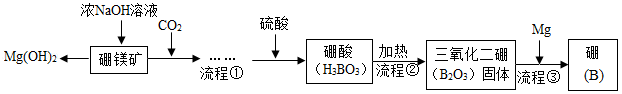
(1)B2O3中B元素的化合价为 。
(2)为加快硼镁矿石与浓NaOH溶液的反应速率,可采取的措施是 ;回收副产物Mg(OH)2可制得流程 的反应物。
(3)H3BO3加热分解只生成两种氧化物,流程②的化学反应方程式为 。
(4)根据流程③的化学反应方程式:B2O3+3Mg 2B+3MgO,理论上制备1.1吨的硼,需消耗镁多少吨写出计算过程)?