配制100g质量分数为16%的Na2CO3溶液,用于演示灭火器原理。回答下列问题。

(1)计算Na2CO3的质量为 g,称量Na2CO3的仪器名称是 。
(2)20℃时,Na2CO3的溶解度为21.5g,⑤中的溶液 (填“是”或“不是”)该物质的饱和溶液。
(3)将烧杯中溶液倒入吸滤瓶的操作是 ,从橡胶管喷出大量液体的原因是 。
(4)酒精(C2H5OH)可作燃料,在空气中完全燃烧的化学方程式是 。酒精燃烧失火,可用干粉灭火器灭火。NaHCO3是干粉的主要成分,俗称是 。用干粉灭火器灭火的正确操作顺序是 → → (填序号)。

实验室有一瓶标签被腐蚀的无色溶液,是稀硫酸和氢氧化钠溶液中的一种。在老师的指导下,小红和小明用不同方法鉴定。
实验一:
|
实验步骤 |
实验现象 |
实验结论 |
|
小红取少量该溶液于试管中,向其中插入没有打磨的铝片 |
开始无明显现象,后产生 |
小红认为该溶液为稀硫酸 |
|
小明用pH试纸测定其pH |
pH=13 |
小明认为该溶液为氢氧化钠溶液 |
小红和小明操作均无误。
【提出问题】
该溶液到底是稀硫酸还是氢氧化钠溶液?
【查阅资料】
铝、氧化铝既能与酸反应,又可与强碱溶液反应,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,氧化铝与氢氧化钠溶液反应生成偏铝酸钠( NaAlO2)和一种氧化物。NaAlO2易溶于水,其水溶液呈碱性,NaAlO2与铝、氧化铝均不反应。
【分析实验得出结论】该溶液为 溶液。
【交流反思】实验一中,小红所做实验开始无明显现象的原因是 。(用化学方程式表示)
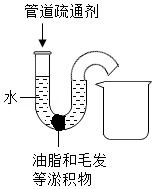
【拓展应用】有一种管道疏通剂,主要成分为铝粉和氢氧化钠粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对油脂和毛发等淤积物的腐蚀,同时产生氢气增加管道内气压,利于疏通。
实验二:小明用如图所示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说明从左端管口加入管道疏通剂,并用胶塞堵住弯管左端上口,可能出现的现象为 (填字母序号)。
A.产生大量气体
B.弯管内温度升高
C.堵塞物变软被气体赶出,落入烧杯中
实验三:为了证明烧杯中废液里是否还含有氢氧化钠,小明做了如下实验
|
实验操作 |
实验现象 |
实验结论 |
|
取少量澄清废液于试管中,滴入酚酞 |
溶液变红 |
废液中有氢氧化钠剩余 |
小红对小明的结论提出了质疑,理由是 ,小红把酚酞改用 (填药品)进行实验,得出废液中还含有氢氧化钠。
管道疏通剂中氢氧化钠过量,可确保铝粉反应完全,并且过量的氢氧化钠对下水道有清污的作用。
如图是实验室气体制取、净化、干燥常用装置图,请根据所给装置图回答问题: 
(1)请写出图中标号①的仪器名称: ;
(2)实验室用高锰酸钾制取氧气,选取的发生装置为 (填字母代号),请写出该反应的化学方程式 ,若用D装置收集氧气,验满方法是 ;
(3)小聪同学在检验二氧化碳时,发现澄清石灰水始终不变浑浊,查找原因得知,制取二氧化碳时所用盐酸浓度过大。为除去二氧化碳中混入的氯化氢体和水蒸气,得到纯净、干燥的二氧化碳,小聪设计了除杂实验。已知:Na 2CO 3+H 2O+CO 2═2NaHCO 3.请你完成装置连接:A→ → →D。
取NaOH和NaCl的混合物3.63克放入烧杯中,加水溶解配制成70克溶液。向该溶液滴加溶质质量分数为7.3%的稀盐酸,测得溶液pH与滴入稀盐酸的质量关系如图所示。
(1)当滴入稀盐酸的质量为11.2克时,溶液的pH 7(填“>”、“<”或“=”);此时溶液中的溶质是 (填化学式)。
(2)当pH=7时,计算该溶液中溶质的质量分数。(写出计算过程)

糖类是人类食物的重要成分,在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成CO2和H2O,同时放出能量(已知每克葡萄糖放出约16kJ的能量)。请回答:
(1)葡萄糖的相对分子质量为 。
(2)葡萄糖分子中碳、氢、氧原子数目比为 (写最简整数比)。
(3)一般人每行走1km,大约需消耗170kJ的能量。假设这些能量全部来自葡萄糖,请问:小明同学步行5km,大约需消耗 克(取整数)葡萄糖。
用如图装置在相应条件下完成下列实验
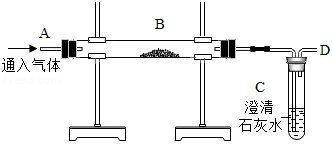
(1)探究燃烧条件:B盛木炭粉。
①由A处通N2一段时间后,加热B,B、C无明显变化。
②待B冷却至室温,由A处通入O2一段时间,B、C无明显变化。
③由A处继续通入O2,加热B,木炭粉燃烧,C中溶液变浑浊。
结论:由①、③可知燃烧需要 ;由②、③可知燃烧需要 。
(2)探究CO与金属氧化物反应:B盛金属氧化物。
I、模拟工业炼铁:A处通CO,B盛Fe2O3粉末,B处下方放酒精喷灯,D处放酒精灯。
实验:在A处通入CO时,应立即点燃 处(填“B”或“D”)酒精(喷)灯。在B处加热一段时间后可观察到的现象是 。
II、探究金属氧化物的组成:A处通CO,B盛金属氧化物,B处下方放酒精喷灯、D处放酒精灯。
已知:CuO、Fe3O4均为黑色物质,B中所盛粉末:CuO或Fe3O4或两者混合物。
实验:同Ⅰ操作、B中可观察到既有红色固体生成,又有黑色固体生成。
实验结论(定性):该黑色粉末为 。
定量分析:经测定反应前B重180克,完全反应后B重170.4克。将反应后B中固体全部加入到足量的稀硫酸中,完全反应后经过滤、洗涤、干燥,测得剩余固体12.8克。
实验结论(定量):m(CuO):m(Fe3O4)= (写最简整数比)。