焰火中的化学
五光十色的焰火让人叹为观止。焰火中的白光主要是由金属镁燃烧产生。如图是有关微粒的结构示意图,请回答下列问题:

(1)燃烧前
图中属于原子的有(填序号) ,属于阴离子的有(填序号) 。氧原子(填"能"或"不能") 直接构成物质。保持金属镁化学性质的微粒是(填符号) 。
(2)燃烧中
在空气中点燃镁条,镁主要跟氧气反应,还能跟氮气反应生成少量氮化镁(氮元素显﹣3价)。
①镁跟氧气反应的微观实质是 。镁跟氮气反应的化学方程式为 ,所属基本反应类型为 。
②焰火中燃烧金属镁是为了把 能转化为 能。
(3)燃烧后
氧化镁能跟盐酸反应生成氯化镁。要把氯化镁中的镁元素重新分配到其它物质中,从化学变化中镁元素化合价是否改变的角度,反应可分为两类,请举例说明(用化学方程式表示) 和 。但无论化学反应多么复杂,从宏观看 不会消失,从微观看 不会消失。
指出下图中倾倒液体药剂时的错误:
⑴_______________________________
⑵_______________________________
⑶_______________________________
⑷_______________________________
指出下列操作导致的后果。
⑴ 把块状固体药品直接丢入试管底部,后果是 。
⑵ 使用胶头滴管后,未经清洗就吸取别的试剂,后果是 。
⑶ 用燃着的酒精灯点燃另一只酒精灯,后果是 。
⑷ 加热液体时,试管口朝着有人的方向,后果是 。
结合下列图示实验装置,回答有关问题:
(1)实验室用高锰酸钾制取氧气时,应选用的发生装置是(填字母下同),反应的化学方程式为,试管口放一团棉花的作用是。
(2)实验室制取二氧化碳时,应选择的发生和收集装置是。
(3)F中观察到的实验现象是。
反应的化学方程式为。
(4)G实验中说明二氧化碳具有的性质是,故
可用于。
(5)常温下,硫化氢(
)是一种有臭鸡蛋气味的气体:实验室可用硫化亚铁(
)固体和稀硫酸反应制得,该反应的化学方程式为
.实验室制取硫化氢气体应选用的发生装置是,依据是。
铝、铁、铜是我们生活中常见的金属。
(1)铝制品具有很好的耐腐蚀性能,原因是。
(2)铁生锈的条件是,生活中防止铁生锈的方法有
(写一种即可)。
(3)高炉中以赤铁矿(主要成分氧化铁)为原料炼铁的原理是(用化学方程式表示)。
(4)为探究铝、铁、铜三种金属的活动性顺序,甲、乙、丙三位同学设计了如下实验方案(金属片已打磨),如图所示: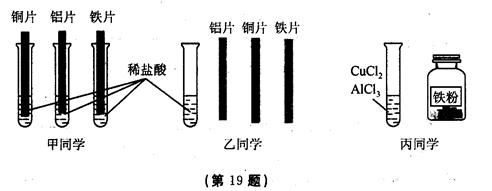
①甲同学根据铜片表面无变化的现象,判断出三种金属的活动性顺序为
。
②乙同学只用一支试管,取一次稀盐酸也能证明
。他在稀盐酸中插入金属的顺序为:或,写出其中一个反应的化学方程式。
③丙同学把一定量的铁粉放入
和
的混合溶液中,充分反应后过滤,向滤出的固体中加入稀盐酸,无明显现象,则滤液中一定含有的溶质是。
(6分)化学与能源、环境关系密切。请你用学过的化学知识回答下列问题:
(1)化石燃料包括煤、、天然气。
(2)煤的气化是高效、清洁利用煤的重要途径。可将煤炼成焦炭,再将焦炭在高温下与水蒸气反应,得到
和
。该反应的化学方程式为,基本反应类型是。
(3)化石燃料燃烧时会产生
气体,
气体的大量排放引起的环境问题是。
(4)化石燃料是不可再生的能源,可开发和利用的新能源有(写一种即可)。
(5)"绿色化学"的特点之一是在化工生产中尽可能实现"零排放"。
和
可以按不同比例反应,生成下列有机物。用
和
反应,只生成一种产物并且能实现"零排放",这种产物是下列物质中的(填字母)。
| A. | 甲酸( ) | B. | 乙酸( ) | C. | 乙醇( ) | D. | 丙酮( ) |