a、b、c、d为短周期元素,a的原子中只有1个电子, 和c +的电子层结构相同,d与b同族.下列叙述错误的是( )
| A. | a与其他三种元素形成的二元化合物中其化合价均为+1 |
| B. | b与其他三种元素均可形成至少两种二元化合物 |
| C. | c的原子半径是这些元素中最大的 |
| D. | d与a形成的化合物的溶液呈弱酸性 |
已知X、Y、Z 3种主族元素在元素周期表中的相对位置如右图所示,设X的原子序数为a,则下列说法中不正确的是()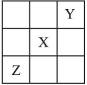
| A.Y与Z的原子序数之和可能为2a | B.Y的原子序数可能为a-17 |
| C.Z的原子序数可能为a+31 | D.X、Y、Z一定都是短周期元素 |
X、Y、Z三种非金属元素具有相同的电子层数,它们的气态氢化物的稳定性强弱顺序是XH3<H2Y<HZ,下列说法中正确的是()
| A.原子序数X>Y>Z | B.原子得电子能力X<Y<Z |
| C.原子半径X<Y<Z | D.离子还原性X3-<Y2-<Z- |
酸雨给人类带来了种种灾祸,严重地威胁着地球的生态环境,下列有关减少或者防止酸雨形成的措施可行的是()
①对燃煤进行脱硫②对含SO2、NO2等工业废气进行无害处理后,再排放到大气中③人工收集雷电作用所产生的氮的氧化物④飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等
| A.①②③④ | B.①②③ | C.①②④ | D.①③④ |
下列关于氯水的叙述正确的是()
| A.新制氯水中既有分子又有离子 |
| B.新制氯水在光照的条件下,可以产生气体,该气体是氯气 |
| C.新制氯水中滴加硝酸银溶液,没有任何现象 |
| D.新制氯水不能使干燥的布条褪色 |
38.4 mg铜与一定量的浓硝酸反应,铜全部反应后,共收集到气体22.4 mL(标准状况),反应消耗硝酸的物质的量是()
| A.1×10-3 mol | B.1.6×10-3 mol | C.2.2×10-3 mol | D.2.4×10-3 mol |