20℃时,将等质量的A、B两种固体物质,分别加入盛有100g水的烧杯中,充分搅拌后现象如图①,加热到60℃时现象如图②,A、B两种物质的溶解度曲线如图③。请结合如图所示回答下列问题:
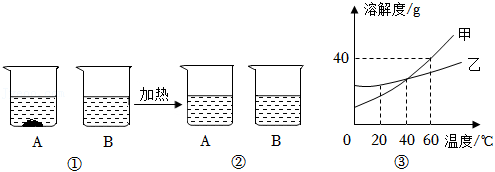
(1)图①中一定为饱和溶液的是 (填“A”或“B”)。
(2)图②中A、B两种溶液中溶质的质量分数的大小关系为A B(填“>”、“<”或“=”)。
(3)图③中表示物质A的溶解度曲线是 (填“甲”或“乙”)。
(4)当温度为 ℃时,A、B两种物质的溶解度相等。
(5)60℃时,要使A、B的饱和溶液析出等质量的固体,需恒温蒸发掉水的质量较多的是 (填“A”或“B”)的饱和溶液。
人类维持生命和健康必须摄取食物。
(1)下列食物富含糖类的是(填字母序号)。
(2)饼干中常添加碳酸钙,其作用是 。
(3)化肥对提高粮食产量具有重要的作用。尿素[CO(NH2)2]是一种常用的化肥,工业上生产尿素的反应的微观示意图如下: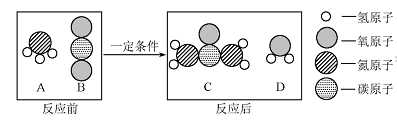
①尿素由种元素组成,属于(填“氮”、“磷”或“钾”)肥。
②生产尿素的反应中,A与 B的质量比为。
写出下列物质的化学式:
(1)纯碱 ;(2)西气东输的气体 ;(3)常用作人工降雨的物质;(4)人体中含量最多的金属元素;(5)目前使用量最大的金属。
(5分)海水中蕴含着80多种元素,海洋是一座巨大的宝库。氯碱工业以海水为原材料可以大量制取烧碱和氯气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产。所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域。
(1)氯碱工业中发生反应的化学方程式为:2NaCl+2H2O=2NaOH+Cl2↑+A,则A的化学式为。氯气常用于自来水的杀菌消毒,它与水反应生成盐酸和次氯酸(HClO),试写出该反应的化学方程式。
(2)下图是甲、乙两种固体物质的溶解度曲线。 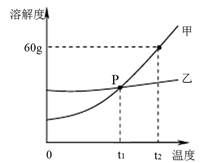
①P点的意义是。
② 甲物质中含有少量乙物质,提纯甲物质可用方法(选填“降温结晶”、“蒸发结晶”之一)。
③t2℃时,甲的饱和溶液中溶质的质量分数是。
(4分)碳元素是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关。
(1)小刚同学对碳及其重要化合物知识进行归纳、整理,并建构了如图所示的转化关系图。请回答下列问题: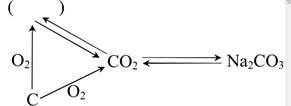
①写出括号内一种含有碳元素物质的化学式;
②写出一个由CO2→Na2CO3反应的化学方程式;
(2)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰(MnCO3),其中锰元素的化合价为。
(3)“碳海绵”是已知最轻的固体材料,由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是(填字母)
A.可燃烧 B.可重复使用 C.可处理海上石油泄漏
(4分)口香糖是以天然树胶或甘油树脂为基础,加入糖浆、薄荷、甜味剂等调和压制而成的,是很受世界人民喜爱的一种休闲食品。随着食品技术的进步以及人们对健康的追求越来越高,口香糖从传统的 “泡泡糖”逐渐发展为今天的木糖醇口香糖。
(1)聚醋酸乙烯酯作为口香糖基质能制造良好的口感,是口香糖中最具有代表性的原料,它的化学式为(C4H6O2)n请你判断该物质属于___________(选填“有机物”、“无机物”、“单质”、“混合物”之一)。
(2)口香糖中的香料质量也是决定口香糖商品价值的重要原因之一,薄荷油是一种极佳的香料,气味清香提神明目,薄荷油主要成分为左旋薄荷醇(其化学式为C12H20O),试计算左旋薄荷醇中碳元素与氢元素的质量比___________(填最简整数比)。
(3)目前,市场上畅销的以木糖醇为原料的口香糖,对修复蛀牙有所帮助。木糖醇的化学式为C5H12O5,其中元素的质量分数最大的是元素。
(4)以下做法中不正确的是________
A.适量咀嚼口香糖可以锻炼面部肌肉
B.吃过的口香糖用纸包好后扔进垃圾桶
C.青少年儿童可以无节制的食用口香糖