某化肥厂生产的一种化肥包装袋上的部分说明如图所示。化学兴趣小组为测定其纯度,做了以下实验(杂质溶于水,且不与硝酸银溶液反应),请根据如图所示的实验过程和提供的数据进行计算。
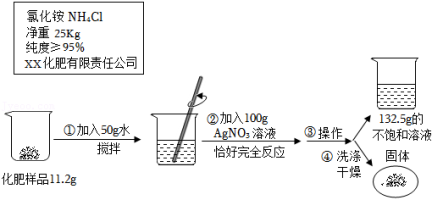
(1)过滤后最终所得固体的质量为 g;
(2)所用硝酸银溶液的溶质质量分数是多少?(写出计算过程)
(3)该化肥是否合格?(写出计算过程,计算结果精确到0.1%)
工业上欲用NaOH溶液处理含204 t Al2O3的铝土矿(杂质不参与反应),反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O。计算:需要消耗NaOH的质量。
有碳酸钠和硫酸钠的固体混合物共40.0克,将它放入98.0克20.0%的硫酸溶液中,充分反应后溶液恰好呈中性,求:(计算结果均保留一位小数)
(1)碳酸钠的质量;
(2)反应后溶液的溶质质量分数。
将25 g石灰石放入烧杯中,加入100 g稀盐酸恰好完全反应(杂质不溶解,也不参加反应),此时烧杯中物质的总质量比反应前减少了8.8 g,计算:
(1)石灰石中碳酸钙的质量分数?
(2)生成物溶液中溶质的质量分数?(结果保留为0.1%)
钢铁是应用广泛的金属材料。
(1)炼铁的主要原理是:在高温下,用一氧化碳将铁从铁矿石里出来。
(2)工业炼铁的原料是:铁矿石、焦炭、、空气;磁铁矿主要成分的化学式是:;炼铁高炉中焦炭通过两步反应转化为CO,这两步反应是:C+O2 CO2 和。
CO2 和。
(3)某钢铁厂每天消耗5000t含氧化铁73.5%的赤铁矿石,则该厂理论上可日产含铁98%的生铁的质量是多少?
敏敏同学为探究石灰石中碳酸钙的质量分数(杂质不与稀盐酸反应),向6.0g石灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体的体积为1.11L(该条件下二氧化碳的密度为1.977g/L)
(1)该反应生成二氧化碳的质量为多少克(精确到0.1g)
(2)该石灰石样品中碳酸钙的质量分数为多少?(精确到0.1%)