实验室常用的干燥剂分碱性、酸性、中性三种类别。碱石灰是一种常用的碱性干燥剂,其成分为 和 ,它吸水能力强,不能干燥二氧化碳气体,在实验室应密封保存。
【学习交流】碱石灰不能干燥二氧化碳气体的原因分析
原因一:氢氧化钠与二氧化碳反应生成碳酸钠;
原因二: 。
实验室有一瓶因敞口久置后变质的碱石灰,某化学兴趣小组对其成分展开讨论与探究:
【提出猜想】变质的碱石灰除含水以外,可能还含有哪些成分?
猜想一:
猜想二:
猜想三:
猜想四:
猜想五:
【提出质疑】
兴趣小组部分同学认为猜想 不合理,应改为 。
【查阅资料】兴趣小组为了更好地进行实验探究,将常见盐的水溶液的酸碱性整理如下:
|
氯化钠 |
硝酸钠 |
碳酸钠 |
氯化钙 |
硝酸钙 |
氯化钡 |
硝酸钡 |
硫酸铜 |
|
中性 |
中性 |
碱性 |
中性 |
中性 |
中性 |
中性 |
酸性 |
【实验探究】
取少量碱石灰样品于试管中,加入足量蒸馏水。
(1)若发现样品完全溶解,则证明猜想 正确;
(2)若发现样品未完全溶解,过滤后得到滤渣M和溶液N,进行相关实验。
实验一:向溶液N中先滴加几滴酚酞溶液,可观察到溶液 ,仅根据此现象不能证明任一猜想是否正确,原因是 ,在此基础上,应如何设计实验证明猜想五正确?请写出实验操作及现象: 。
实验二:向滤渣M中加入适量盐酸,可看到有气泡产生,反应方程式为 。
【拓展延伸】干燥剂的选择要视被干燥气体的性质而定,碱性干燥剂不能干燥酸性气体,同理,酸性干燥剂不能干燥碱性气体。总之,干燥剂不能与被干燥气体发生化学反应。
【2015年福建省厦门市】“史上最贵”的实验:
步骤Ⅰ.让金刚石在充足的氧气中燃烧,收集生成的气体;
步骤Ⅱ.让足量镁条在步骤Ⅰ生成的气体中燃烧,生成黑色的炭粉和白色的固体氧化物。
(1)步骤Ⅱ中发生反应的化学方程式:___________________,基本反应类型是_________。
(2)若金刚石质量为m1,按上述步骤反应且转化完全,生成的炭粉质量为m2,则m1____m2(填“<”、“=”、“>”=,理由为___________________________________________。
【2015年安徽省】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式 。
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律。
我 (“同意”或“不同意”)小明的观点,因为 。
(3)小红按下图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。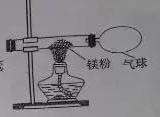
【提出问题】黄色固体是什么呢?
【查阅资料】
①氧化镁为白色固体
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体为Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 |
实验现象及结论 |
【反思与交流】空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁,为什么?请给出合理的解释 。
[注意:若答对第(4)小题奖励4分,化学试卷总分不超过60分。]
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
| 实验序号 |
实验1 |
实验2 |
实验3 |
|
| 与镁条反应的溶液 |
NH4Cl |
NaCl |
Na2SO4 |
H2O |
| 实验现象 |
有大量气泡产生 |
有较多气泡产生 |
有少量气泡产生 |
气泡较少 |
| 加热后,实验现象 |
气泡明显增多, 可闻到氨味 |
气泡增多 |
气泡增多 |
气泡增多 |
上表中,用水进行实验的目的是 。
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分)
①
②
③
化学与"美丽厦门"
(1)化学让天更蓝
①汽车尾气处理中使用了催化剂,该催化剂中某元素在元素周期表中的部分内容如图所示,从中获取一条信息:_______________________________。 
②公交车使用天然气等清洁能源,写出天然气主要成分燃烧的化学方程式: ___________________________。
③未来氢能源汽车可实现零污染。在催化剂、光作用下,水分解获得氢能源,写出该方法获得氢能源的化学方程式: ________________________________。
(2)化学让水更洁净
①生活污水截流处理过程如图所示,其中采用的净水方法有____________(写出一种)。 
②如图是从海水中获取淡水的一种装置,请从能源角度指出其优点:________________________________。 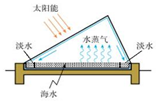
③检验上述所获取的水是否为硬水,常用试剂是_________。
【2015年四川省成都市】(9 分)自来水厂净水过程的主要操作流程如下图:
资料:常用的絮凝剂有明矾[KAl(SO4).12H2O],消毒剂有液氯(Cl2)
回答下列问题:
(1)操作X 的名称是 ,试剂A 的名称是 。
(2)明矾作絮凝剂是因为与水反应生成氢氧化铝胶状物。氢氧化铝的化学式为 。
液氯与水中杂质反应生成一些对人体有害的物质,例如三氯甲烷(CHCl3).三氯甲烷属于_______(填“有机物”或“无机物”)
(3)高铁酸钾(K2FeO4)能作消毒剂与絮凝剂。它杀菌时会生成氢氧化铁胶状物。高铁酸钾中铁元素的化合价是 。
(4)硫酸铝也能做絮凝剂,写出制取硫酸铝反应的化学方程式________________________
(5)自来水厂的净水过程 (填“能”或“不能”)将硬水软化成软水,生活中将硬水软化的方法是 。
【2015年山东省济南市】济阳仁风镇是“中国西瓜之乡”,生产的富硒西瓜色泽好、糖分高、口感佳,被农业部认证为国家级“无公害农产品”和“绿色食品”。
(1)西瓜适合在弱酸性土壤中生长。某校化学课外小组的同学,为了考查某地土壤是否适合种植西瓜,对其土壤进行了实验分析。具体实验步骤如下:
①将在该地多点选取的土样混合,并研成粉末状。
②称量一定质量的土壤粉末置于烧杯中,加入适量水,搅拌。
③将充分溶解后的混合液进行过滤,所使用的装置如右图所示,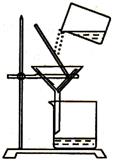
请指出图中的一项错误:_______________________________________。
④用pH试纸测定过滤后所得土壤溶液的pH,测定的具体方法是____________________。
(2)经测定,该土壤溶液的pH为8。为适合西瓜种植,需对该土壤的酸碱性进行调节。则下列各项中,可采用的是____(填选项序号)。
①施以氢氧化钙粉末 ②施以碳酸钙粉末 ③用氨水进行喷灌 ④适量施用酸性肥料
(3)硒(Se)是人体所需要的重要矿物质营养素,有“抗癌之王”的美称。硒的原子序数为34,其相对原子质量为79,硒原子最外电子层上有6个电子。则下列说法中,不正确的是_________(填选项序号)。
①硒为非金属元素 ②一个硒原子的原子核内有34个质子
③硒原子很容易失去电子 ④富硒西瓜中的硒元素以化合物形态存在