某校进行化学实验技能比赛,实验桌上准备了部分仪器和用品,如图所示:

(1)如图中仪器A的名称是 。
(2)甲同学要进行“实验室制取并收集二氧化碳”的操作,可从如图中选择的仪器有(填数字序号) 。
(3)乙同学要进行“粗盐提纯”中的“过滤”操作,除如图中提供的仪器外,还需要增加一种仪器,这种仪器的作用是 。
(4)以下是丙同学进行“实验室制取并收集氧气”实验的主要操作步骤,这些步骤的正确顺序是(填字母序号) 。
| A. |
添加药品 |
| B. |
清洗仪器,整理实验台 |
| C. |
收集气体 |
| D. |
检查装置的气密性 |
制盐在我国有着悠久的历史。某盐湖水样品含有 及少量 和 ,某小组从中获取 和 的主要过程如下:

(1)“除杂1”应依次加入的两种试剂是______、______,“除杂2”应加入的试剂是______。(除杂限选试剂: )
(2)将“溶液A”在 蒸发浓缩,至有少量固体析出。

①该小组分析溶解度曲线,推测析出的少量固体是 ,但检验后却发现是 。请作出合理解释:______。
②该小组停止蒸发浓缩,经______、过滤得到大量 固体及母液;将母液中的 分离出来,操作是______。
(3)设计由硫磺(单质硫)生产 的转化路径,依次写出反应的化学方程式:______。(提示:常见 价硫的化合物可与 化合为 价硫的化合物)
电解水制氢联合碳酸钙分解制备氧化钙,能减少碳排放,助力碳中和。该新方法的示意图如图所示。
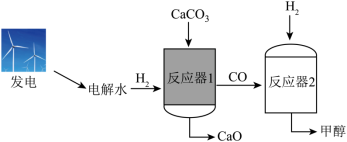
(1)传统方法: 在 以上完全分解生成 和__________(填化学式)。
(2)新方法:
i.电解水属于_____反应(填基本反应类型),反应前后氢元素的化合价_____(填“升高”“降低”或“不变”)。
ii.反应器1:一定的 环境及较低温度下 可与 反应生成 和 。 与 的分子个数比为_______。
还可以直接分解。反应器1中 、 的含量随反应温度的变化如下图所示。________ 时,抑制 生成的效果最好。

iii.反应器2:一定条件下, 与 发生化合反应生成甲醇( ),化学方程式为_________ 。
(3)与传统方法相比,新方法的优点有__________________________(写两条)。
[基础实验与学科实践]
回答下列问题。
(1)实验室制取 及性质检验

i.上图中仪器 的名称是__________。
ii.用高锰酸钾制取 ,应选择上图中的发生装置_______(填字母)。化学方程式为__________。
iii.收集一瓶 并进行性质检验。
|
操作 |
现象 |
结论 |
|
|
硫燃烧时,_____(填字母),生成刺激性气味的气体 a.产生大量白烟 b.生成黑色固体 c.发出蓝紫色火焰 |
具有氧化性 |
|
集气瓶中 溶液的作用是_________________ |
||
(2)制作氧自救呼吸器

查阅资料,超氧化钾( )为黄色固体,分别与 反应生成 和白色固体、产氧效率高,适合作生氧剂。
①原理分析: 、 则 的化学式为__________。
②动手实践:设计并制作氧自救呼吸器,如图所示,使用一段时间后,观察到生氧剂由______(填颜色变化),则基本失效。
草木灰是作物秸秆、枯枝等燃烧后的剩余灰烬,也是农业生产钾肥的重要来源之一,课外实验小组为探究草木灰的成分进行了下面实验:
①将一定量的草木灰放入烧杯,加入足量蒸馏水浸泡,经过滤获取澄清滤液。浸泡的目的是 ;
②取少量上述滤液,滴加氯化钡试剂,有白色沉淀生成,初步判定滤液中可能含有 (填符号);继续滴加稀盐酸,沉淀全部溶解,将产生的气体通入澄清石灰水出现白色浑浊。分析实验可知,草木灰提供钾肥的主要成分是 (填化学式);
③已知滤液呈碱性,请设计实验证明:
|
实验步骤 |
现象与结论 |
|
|
|
人体呼出气体中主要含有氮气、氧气、水蒸气、二氧化碳。为验证人体呼出气体的成分,某兴趣小组利用下面装置进行实验。

请回答:
①呼出气体通过装置A可观察到 ,目的是 ;
②随反应进行,装置中铜网逐渐变为黑色,其反应的化学方程式为 ;
③装置D出现白色浑浊,证明呼出的气体中含有 ;
④E装置的作用是 ,尾气的主要成分是 。