为了保护生态环境,针对全球气候变化,中国政府向全球承诺,力争于2060年前实现“碳中和”。“碳中和”是指在一定时间内,使二氧化碳的排放总量与吸收总量平衡,实现“零排放”。实现“碳中和”通常可采取如下措施:
Ⅰ.碳减排:减少人类生产和生活中二氧化碳的排放量。
(1)下列做法不能实现“碳减排”的是 。
A.加高烟囱排放工业废气
B.推进新能源汽车使用
C.废弃物分类投放并回收利用
D.养成节约用水用电习惯
Ⅱ.碳吸收:①利用植物光合作用,这是自然界消耗二氧化碳的最重要途径;②利用“碳捕捉与封存技术”,即通过一定的方法,将工业生产中产生的 分离出来进行储存。在实际生产中,经常用 溶液来“捕捉” 流程如图所示(部分条件及物质未标出)。
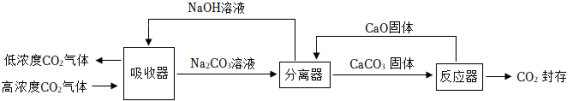
(2)用该技术进行“碳捕获”有效利用了原材料,该过程中被循环利用的物质有 。
(3)分离器中发生的反应:① ,② 。现有溶质质量分数为10.6%的 溶液100千克,求完全反应后,理论上可生成 的质量(要求根据化学方程式计算)。
Ⅲ.碳转化:指二氧化碳的资源化利用。
超氧化钠(NaO2)是一种固体供氧剂,可应用于家庭急救,其供氧的原理是4NaO2+2H2O=4NaOH+3O2↑.为探究长期存放的超氧化钠固体是否变质,进行如下实验:
I.取少量固体,加入足量稀盐酸,观察到有气泡生成。
Ⅱ.另取少量固体,用足量水溶解后,加入一定量氢氧化钙溶液。实验过程中只观察到有白色沉淀生成。
(1)I中现象能否判断超氧化钠已变质?说明理由。
(2)Ⅱ中现象可得出固体中一定含有 ,一定没有 。若要进一步确定其成分,可取少量固体充分溶解后继续实验,需用到的试剂有 。
(3)将I、Ⅱ中反应后的物质倒入同一烧杯中,一段时间后,得到澄清溶液。写出溶液中溶质成分可能存在的情况。
在实验室利用以下装置制取气体 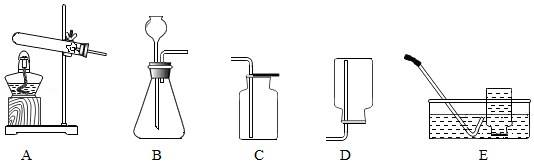
(1)用高锰酸钾制氧气的化学方程式为 。为了得到相对纯净的氧气,收集装置应选 (填字母序号,下同),检验收集到的气体为氧气的操作是 。
(2)用过氧化氢溶液制氧气的化学方程式为 。发生装置应选 ,选择该装置的原因是 。
汽车给人们的生活带来方便的同时,也带来节能和减排的问题。如图是某种汽车的燃料燃烧过程示意图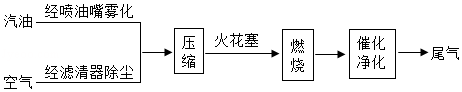
(1)从燃烧的条件看,火花塞的作用是 。
(2)将汽油与空气的混合气充分压缩,有助于节省燃料,说明主要原因。
(3)乙醇的含碳量比汽油的低。分析在汽油中加入适量乙醇,对尾气中炭黑排放量的影响。
(4)利用催化净化装置,可使燃烧过程中产生的CO和NO在催化剂的作用下,转化为两种空气中常见的无害气体,该反应的化学方程式为 。
某兴趣小组在实验室里做制取氢气的实验,取6.5g锌和93.7g稀硫酸放入同一烧杯中,恰好完全反应。请计算:(写出计算过程)
(1)生成氢气的质量
(2)反应后所得溶液中溶质的质量分数。
食用“碘盐”是消除碘缺乏症的最有效方法。“碘盐”就是在食盐中加入一定量的碘酸钾(KIO3)。回答下列问题:
(1)“碘盐”中的碘主要指 (填字母序号)。
A.碘单质 B.碘元素 C.碘原子 D.碘分子
(2)碘酸钾中碘元素的质量分数为 (计算结果精确到0.1%)