定律是对自然现象或关系的描述,通常可用数学方式加以表达。在学习“质量守恒定律”时,小丽查阅到以下材料:
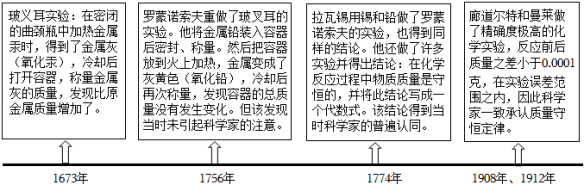
(1)玻义耳实验中,金属灰增加的质量是 ;
(2)质量守恒定律的发现过程,带给我们的启示有 (填字母);
A.要善于总结前人的成果和经验
B.实验的成功与否,取决于药品的选择
C.定量方法是科学研究的重要方法
受上述研究启发,小丽对相关实验进行了深入探究。
(3)在白磷燃烧前后质量测定实验中(如图),气球的作用有 ;

(4)小丽认为,蜡烛燃烧后剩下的固体质量比燃烧前少了,因此该现象不符合质量守恒定律。请你设计一个能说服小丽的简明实验思路 。
如图是初中化学常用的实验装置,请回答下列问题。

(1)仪器①的名称 。
(2)实验室制取O2、CO2、H2均可选择 (填装置代号)作为气体的发生装置。
(3)实验室不使用催化剂就能制取O2的化学方程式为 ,属于 反应(填“化合”“分解”“置换”或“复分解”)。
(4)实验室制取二氧化碳的化学方程式为 ,若要收集干燥的二氧化碳气体则需要将E装置中 端与D装置中 端相连接(填导管口字母代号)。
(5)某气体可用C装置来收集,因为该气体 。
(6)组装A装置时,应遵循 (填“从上往下”或“从下往上”)的顺序操作。
了解溶液的酸碱性,学会测定溶液酸碱度对于生活、生产以及人类的生命活动具有重要的意义。请回答下列问题。
(1)测定溶液的酸碱度时,用干净的玻璃棒蘸取待测液滴在 上,然后再与标准比色卡对照,得出该溶液的pH。
(2)测得家庭生活中常用的炉具清洁剂pH 7(填“<”“=”或“>”)
(3)某盐酸溶液pH=3,要使其pH>7可采用的方法是 。
请根据下列实验装置图,回答有关问题:

(1)请写出图中仪器的名称:a ;
(2)若用A装置作为实验室制取氧气的发生装置,反应的化学方程式是 ,若用D装置收集,验满的方法是 ;
(3)实验室可用 (填一个字母序号)装置作为发生装置制二氧化碳,该装置的主要优点是 ;
(4)若用G装置收集一瓶干燥的某气体,则该气体不可能是 (填字母序号)。
a.CH 4 b.H 2 c.O 2 d.CO 2
如图是初中化学的一些基本实验,请回答相关问题:

(1)A实验是用烧杯罩住点燃的蜡烛,说明燃烧必须具备的条件之一是 ;
(2)B装置是电解水的实验,实验得出水由 组成;
(3)C实验是蒸发食盐水的实验,蒸发时用玻璃棒不断搅拌的目的是 ;
(4)根据D实验中得出的二氧化碳的有关性质,可知二氧化碳可用于 。
化学兴趣小组的同学在探究碱溶液的化学性质时,进行了如图所示的实验。

(1)实验A中,推入NaOH溶液后,可观察到的现象是 。
(2)实验B中发生反应的化学方程式为 。
实验结束后,小组同学对B试管中上层清液的溶质成分产生疑问,作出猜想:
猜想一:只含有NaOH;猜想二:含有NaOH、Na 2CO 3;猜想三:含有NaOH、Ca(OH) 2同学们取少量B试管中的清液分别置于甲、乙两支试管中,进行探究:
|
实验操作 |
实验现象 |
结论 |
|
在试管甲中滴加碳酸钠溶液 |
不产生白色沉淀 |
猜想三错误 |
|
在试管乙中滴加足量稀盐酸 |
|
猜想二正确 |
(3)A、B、C、D四个实验中能体现碱化学通性的是 (填字母)。小组同学经过讨论认为A、B、C、D四个实验并没有探究出碱所有的化学通性,从这四个实验中选择一个,继续加入相关试剂,能得出碱的其它化学通性,实验的方案是 (写出操作和现象)。