化学兴趣小组的同学在探究碱溶液的化学性质时,进行了如图所示的实验。

(1)实验A中,推入NaOH溶液后,可观察到的现象是 。
(2)实验B中发生反应的化学方程式为 。
实验结束后,小组同学对B试管中上层清液的溶质成分产生疑问,作出猜想:
猜想一:只含有NaOH;猜想二:含有NaOH、Na 2CO 3;猜想三:含有NaOH、Ca(OH) 2同学们取少量B试管中的清液分别置于甲、乙两支试管中,进行探究:
实验操作 |
实验现象 |
结论 |
在试管甲中滴加碳酸钠溶液 |
不产生白色沉淀 |
猜想三错误 |
在试管乙中滴加足量稀盐酸 |
|
猜想二正确 |
(3)A、B、C、D四个实验中能体现碱化学通性的是 (填字母)。小组同学经过讨论认为A、B、C、D四个实验并没有探究出碱所有的化学通性,从这四个实验中选择一个,继续加入相关试剂,能得出碱的其它化学通性,实验的方案是 (写出操作和现象)。
如图是实验室制取氧气并验证氧气化学性质的部分装置.请回答有关问题.

(1)仪器a的名称是 .
(2)用高锰酸钾制取一瓶较纯净的氧气,应选择的发生和收集装置是 ,写出该反应的化学方程式 .
(3)实验室用C装置收集二氧化碳气体时,验满的操作是 ,收集二氧化碳气体用装置C而最好不用E的原因是 .
请根据如图实验回答问题.
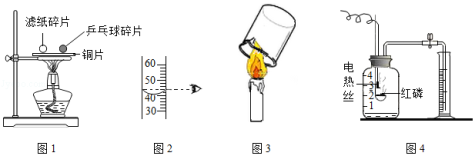
(1)图①中先燃烧的物质是 .
(2)配制一定溶质质量分数的溶液,按图②所示量取水的体积,当其他操作均正确,所配溶液的溶质质量分数会 (填"偏大"、"偏小"或''无影响).
(3)图③中干而冷的烧杯内壁上有水雾产生,说明石蜡中含有 元素.
(4)图④是测定空气中氧气含量的改进装置(利用电热丝通电放出热量引燃红磷),其优点是 .
观察是学习化学的重要方法。我们可以运用自己的感官,也可以借助仪器通过实验,观察物质及其变化的条件、现象和结果。
观察与思考一:蜡烛在空气中燃烧

观察与思考二:在密闭容器内,蜡烛燃烧过程中O 2体积分数的测定
实验1:一定条件下,蜡烛在一瓶空气中燃烧。某同学利用O 2传感器,测定燃烧过程中O 2的体积分数。(如下图所示)

观察实验结果图,初始时O 2的体积分数是 %,蜡烛熄灭时O 2的体积分数是 %。
实验2:相同实验条件下,某同学另取一瓶混有空气的O 2进行测定(初始时O 2的体积分数是30%)。
结合已有信息,合理猜想:蜡烛熄灭时O 2的体积分数(与实验1相比较)。
请写出两种不同情况并分别说明理由。
【温馨提示:实验操作合理,蜡烛相同且量足够,忽略仪器误差】
猜想1及理由: ;
猜想2及理由: 。
根据表中信息,请回答下列问题:
部分碱、酸、盐的溶解性表(20℃)
|
阴离子 阳离子 |
OH ﹣ |
NO 3 ﹣ |
Cl ﹣ |
SO 4 2 ﹣ |
CO 3 2 ﹣ |
PO 4 3 ﹣ |
|
H + |
溶、挥 |
溶、挥 |
溶 |
溶、挥 |
溶 |
|
|
K + |
溶 |
溶 |
溶 |
溶 |
溶 |
溶 |
|
Na + |
溶 |
溶 |
溶 |
溶 |
溶 |
溶溶 |
|
Ba 2+ |
溶 |
溶 |
溶 |
不 |
不 |
不 |
|
Ca 2+ |
微 |
溶 |
溶 |
微 |
不 |
不 |
|
Cu 2+ |
不 |
溶 |
溶 |
溶 |
﹣ |
不 |
说明:"溶"表示那种物质可溶于水,"不"表示不溶于水,"微"表示微溶于水,"挥"表示挥发性,"﹣"表示那种物质不存在或遇到水就分解了。
(1)CaCO 3属于 (填"可溶物"、"微溶物"或"不溶物")。
(2)表中可溶于水的硫酸盐有 种。
(3)在溶液中,磷酸钠与氯化钙能否发生复分解反应。若能,写出化学方程式;若不能,说明理由。
(4)某同学将盐酸倒入Ba(OH) 2溶液中,得到溶液甲。
①溶液甲中溶质的组成情况可能有 种。
②实验设计:探究溶液甲中可能含有的溶质
a.探究溶液甲中是否含盐酸
|
方案编号 |
实验操作 |
实验现象 |
|
1 |
取少量溶液甲于试管中,加入铁粉 |
是否 |
b.探究溶液甲中是否含Ba(OH) 2
|
方案编号 |
实验操作 |
实验现象 |
|
2 |
取少量溶液甲于试管中,加入 溶液 |
是否产生蓝色沉淀 |
|
3 |
取少量溶液甲于试管中,加入Na 2SO 4溶液 |
是否产生白色沉淀 |
上述三个方案中有一个不合理,请指出不合理的方案编号并说明理由: 。
③欲从溶液甲中获得纯净的BaCl 2固体,应采取的简单操作是 。

如图是实验室制取气体的常用装盆,请回答下列问题:

(1)写出图中标号仪器的名称:a 、b .
(2)实验室可加热KMnO 4固体制取O 2:
①请写出该反应的化学方程式 ;
②如A所示,加热一段时间后,某同学发现试管口未放置棉花团,应采取的正确操作: ,再组装好仪器继续实验.
(3)实验室可用锌粒与稀硫酸反应制取H 2,请写出该反应的化学方程式: ,应选用的装置是 (填字母).
(4)实验室选用C装置制取CO 2的化学方程式:CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑
请计算:
①CO 2的相对分子质量是 ;
②现需收集4 瓶(每瓶0.125L) CO 2气体(实验条件下CO 2的密度为2g•L ﹣ 1),其质量是 g;
③收集上述CO 2至少需要大理石(含CaCO 38O%)的质量是 g (精确到0.1g).