[科学探究]
耕地盐碱化影响粮食安全,盐碱地综合治理与利用可促进农业高质量发展,兴趣小组开展了与土壤盐碱化相关的探究活动。
(1)成因:由农业灌溉或化肥施用引起的土壤盐碱化如图所示,当进入土壤中盐的量超出植物的吸收能力时,随水分蒸发,__________导致土壤盐碱化。
(2)检测:配制土壤样品浸出液、用_______测定、若 、则浸出液显__________性。
(3)探究:某地土壤碱化可能由 、 中的一种两种引起。教师提供模拟盐碱化壤样品浸出液。
[查阅资料] 易溶于水; 为白色固体,难溶于水; 为白色固体,难溶于水和盐酸。
[提出问题]样品中的是什么?
[作出猜想]猜想1:
猜想2:_________
猜想3: 和
[实验探究]
(4)取少量出分别加管A、B中
|
实验序号 |
操作 |
现象 |
结论 |
|
1 |
向A中滴加少量 溶液 |
产生白色沉淀 |
含 |
|
2 |
向B中滴加过量稀盐酸 |
_______ |
含 |
[分析评价]
(5)有同学认为实验1不够严谨,理由是______________(用化学方程式解释)
[补充实验]
(6)
|
实验序号 |
操作 |
现象 |
结论 |
|
3 |
向实验2反应后的溶液中滴加少量 溶液 |
_______ |
猜想3成立 |
(7)交流:应对土壤盐碱化的合理措施有___________(多选,填字母)
| A. |
合理施肥 |
B. |
引海水灌溉 |
C. |
用熟石灰改良 |
D. |
种植耐盐碱作物 |
(1)目前世界上一半以上的铜用于电力和电信工业,是因为铜具有(填字母)
A.导热性B.延展性 C.导电性 D.金属光泽
(2)我国第四套人民币的硬币从1999年开始发行,一元为钢芯镀镍(Ni ),五角币为钢芯镀铜合金,一角币为铝合金或不锈钢。在选择铸造硬币的材料时需要考虑的因素有 (选填序号)。
A.金属的导电性 B.金属的耐腐蚀性
C.金属的硬度与耐磨性 D.金属价格与硬币面值的吻合度
①镍能与盐酸或稀硫酸反应,生成可溶于水的正二价镍的化合物,并放出氢气。其反应没有铁与酸反应剧烈。镍与盐酸反应的化学方程式为.
②用镍片、硫酸亚铁溶液和溶液做实验也能判断Ni、Fe、Cu的金属活动性顺序。三种金属的活动性顺序为。
(3)若将一定质量的Zn放入CuCl2和MgCl2的混合溶液中,充分反应后过滤,所得滤液中一定含有的溶质(可溶性化合物)是。
(4)活动课上小明将一枚五角币放在酒精灯火焰上加热片刻,发现表面变黑。
【假设与预测】假设I.五角币加热变黑,是因为酒精灯内焰的黑烟附着在五角币的镀铜上;
假设II.五角币加热变黑,是因为五角币上的镀铜与 ______发生了化学反应。
【实验与事实】
实验一:用洁净的干布擦一擦五角币上的黑色物质,黑色物质不易被擦去;再另取一枚五角币放在石棉网上,用酒精灯加热片刻,五角币也变黑。
实验二:取一块铜片放入小试管中并塞上橡皮塞,然后用酒精灯加热直至试管中铜 片变黑;再将铜片反转到另一面,加热片刻,铜片不再变黑。
【解释与结论】上述实验一和实验二证实,假设 不成立。
【表达与交流】铜片在空气中加热,发生的化学反应方程式为 。
天然气作为燃料已进入千家万户,其主要成分是CH4,它在空气中完全燃烧生成CO2和H2O。如果它不完全燃烧会生成什么物质呢?某研究小组对此展开探究。
请写出CH4完全燃烧的化学方程式 ____________________________,
[猜想]由此推测生成物中一定有H2O,可能有的气体 ①CO2②CO③CO2 CO
[实验探究]该小组将生成的混合气体依次通过下图所示装置,验证猜想。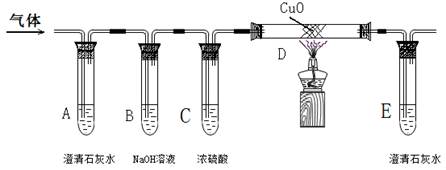
(1)若猜想③成立,则该实验中有__________________________________________的现象。
(2)若混合气中有CO,D中发生的化学方程式为___________________________________.
(3)小文提出:从环保角度看,此装置有一个不足之处,你认为是______________________.
某校化学实验兴趣小组想了解水的组成,他们做了如下实验:(13分)
【提出疑问】水是由什么元素组成的?
【作出猜想】猜想(1)水是由氧元素组成;猜想(2)水是由氢元素组成;
猜想(3)水是由氢元素和氧元素组成。
【设计实验】[实验]如下图:电解水的实验
【实验现象】
①通电后,两根电极上都出现。
②一段时间后正负两极试管内收集的气体体积比为;
③正极产生的气体是,负极产生的气体是。
【实验验证】本实验中生成的两种气体,你能鉴别吗?试说说:。
【实验结论】①水是由组成的。② 电解水的文字表达式。
【实验反思】通过本实验再次说明了在化学变化中是可分的;反应前后的种类是不变的。
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【查阅资料】电石主要成分为碳化钙(CaC2),它没有可燃性。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:;猜想三:Ca(OH)2。
他的依据是。
【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:
。
【进行实验】(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液,通入,有白色浑浊出现,证明猜想三成立。该反应的化学方程式为:。
结论:白色固体是Ca(OH)2。
【拓展应用】某市一辆满载电石的货车遇大雨引发熊熊大火,其中的可燃物是________,且该反应放出大量热,使可燃物达到_______________。
【交流反思】通过上述实验可知,电石在保存和运输时的注意事项_ ___
早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
(1)写出CO还原Fe2O3的化学方程式_____________________________。
(2)实验中盛澄清石灰水的试管中可观察到的现象是__________________。
(3)右边导气管口放置点燃的酒精灯的目的是__________________________。
(4)实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是__________________________________。