下列反应的离子方程式书写正确的是
| A.稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| B.硫酸铜溶液中加入铁粉反应:Cu2++Fe=Fe2++Cu |
| C.氢氧化钡溶液与稀 H2SO4反应:Ba2++SO42-=BaSO4↓ |
| D.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
a g Mg、Al合金完全溶解在C1 mol·L-1、V1L HCl溶液中,产生b g H2。再向反应后的溶液中加入C2 mol·L-1、V2 L NaOH溶液,恰好使沉淀达到最大值,且沉淀质量为d g。下列关系错误的是
| A.铝为 (24b-a)/9 mol |
| B.C1=C2V2/V1 |
| C.d=a+17b |
| D.与金属反应后剩余盐酸为(C1V1-b)mol |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是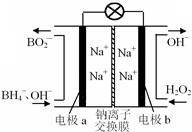
| A.电池放电时Na+从b极区移向a极区 |
| B.电极b采用MnO2,MnO2既作电极材料又有催化作用 |
| C.该电池的负极反应为:BH4-+8OH--8e-=BO2-+6H2O |
| D.每消耗3 mol H2O2,转移的电子为3 mol |
增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得: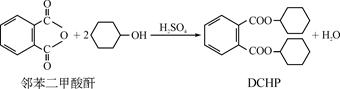
下列叙述正确的是
| A.邻苯二甲酸酐的二氯代物有3种 |
| B.环己醇分子中所有的原子可能共平面 |
| C.DCHP能发生加成、取代、消去反应 |
| D.1 mol DCHP最多可与含2 mol NaOH的烧碱溶液反应 |
短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和。下列说法正确的是
A.元素B和E的氧化物对应的水化物均为强酸
B.C的单质能与A的氧化物发生置换反应
C.元素C、D、E的最高价氧化物对应的水化物之间均可相互反应
D.工业上常用直接电解元素C、D的氯化物来制取它们的单质
下列现象或反应的原理解释正确的是
| 现象或反应 |
原理解释 |
|
| A. |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔对熔化的铝有较强的吸附作用 |
| B. |
合成氨反应需在高温条件下进行 |
该反应为吸热反应 |
| C. |
镀层破损后,镀锡铁比镀锌铁易腐蚀 |
锡比锌活泼 |
| D. |
2CO=C+O2在任何条件下均不能自发进行 |
该反应△H>0,△S<0 |