为了探究镁的性质,在锥形瓶(如图)中注入足量的稀盐酸(其溶质为HCl),在锥形瓶口紧系一气球,气球内盛有一定质量的单质镁碎屑。(提示:Mg+2HCl=MgCl2+H2↑)试根据要求回答下列问题:

(1)将气球内的单质镁全部倒入锥形瓶中。写出观察到的一项实验现象: 。
(2)倒入单质镁,反应结束后,整个装置与之前相比较 (填写下列各项的序号)。
①没有变化 ②有变化,后者质量变小 ③有变化,后者质量变大 ④不能确定
(3)若想制取2 g的氢气,需要镁的质量是多少?
振衡中学校办工厂利用熟石灰与纯碱反应生产工业烧碱,学校化学兴趣小组到校办工厂检验刚生产出的一批产品的纯度(氢氧化钠的质量分数).检验时称取样品20.00g,溶于100.00g水中。向其中逐滴加入氢氧化钡
溶液,当恰好不再产生沉淀(
)时,用去溶质的质量分数为10.0%的氢氧化钡溶液8.55
,试求:
(1)反应中生成的碳酸钡的质量(保留2位小数)。
(2)该批产品中氢氧化钠的质量分数(精确到0.1% )。
(3)反应后所得溶液中氢氧化钠的质量分数(精确到0.1% )。
某钢铁厂用100 含氧化铁80%的赤铁矿炼铁,计算理论上可冶炼出铁的质量。
在某种细菌作用下,氨气(
)和氧气可处理含甲醇(
)的工业废水。
计算下列问题:
(1)
的相对分子质量为;
(2)
中氧气元素的质量分数(写出计算过程)。
某纯碱样品中含有少量氯化钠,取该样品11
,全部溶液在100
水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,
点时,过滤,得到滤液242
,计算: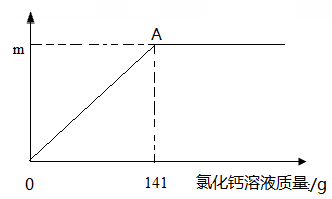
(1)反应生成沉淀的质量
为
。
(2)滤液中溶质的质量分数。
向100g硫酸铜溶液中,逐滴加入
溶液,加入
溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:
(1)将
点所对应的混合物过滤,滤液中所含溶质为;
(2)图中
点所对应的溶液总质量为g;
(3)求(1)中所得滤液的溶质质量分数(请写出计算过程)。