环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
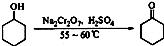
环己醇、环己酮和水的部分物理性质见下表:
| 物质 |
沸点(℃) |
密度(,20℃) |
溶解性 |
| 环己醇 |
161.1(97.8)★ |
0.9624 |
能溶于水 |
| 环己酮 |
155.6(95)★ |
0.9478 |
微溶于水 |
| 水 |
100.0 |
0.9982 |
★括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性溶液氧化环己醇反应的,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性溶液加到盛有环己醇的烧杯中,在55~60℃进行反应。
反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水的混合物。
①酸性溶液的加料方式为。
②蒸馏不能分离环己酮和水的原因是。
(2)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集151~156℃的馏分; b. 过滤;
c. 在收集到的馏分中加NaCl 固体至饱和,静置,分液;
d. 加入无水固体,除去有机物中的少量水。
①上述操作的正确顺序是(填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需。
③在上述操作c中,加入 固体的作用是。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有种不同化学环境的氢原子。
咖啡酸苯乙酯( )是一种天然抗癌药物,在一定条件下能发生如下转化:
)是一种天然抗癌药物,在一定条件下能发生如下转化:
请填写下列空白:
(1)A分子中的官能团是_________________________;
(2)高子M的结构简式是_________________________;
(3)写出A→B反应的化学方程式_________________________;
(4)B→C发生的反应类型有_________________________;
D→E发生的反应类型有_________________________;
(5)A的同分异构体有很多种,其中,同时符合下列条件的同分异构体有__________种。
①苯环上只有两个取代基②能发生银镜反应
③能与碳酸氢钠溶液反应④能与氯化铁溶液发生显色反应
Ⅰ.某无色溶液X,由K+、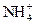 、Ba2+、Al3+、Fe3+、
、Ba2+、Al3+、Fe3+、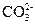 、
、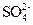 中的若干种离子组成,取该溶液进行如下实验:
中的若干种离子组成,取该溶液进行如下实验: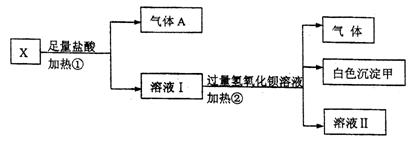
(1)白色沉淀甲是。
(2)试写出实验过程中生成气体A、B的离子方程式、。
(3)通过上述实验,可确定X溶液中一定存在的离子是,要确定可能存在的离子,需补加的实验是。
Ⅱ.A、B、C三种强电解质,它们在水中电离出的离子如下表所示: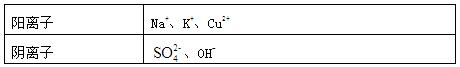
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。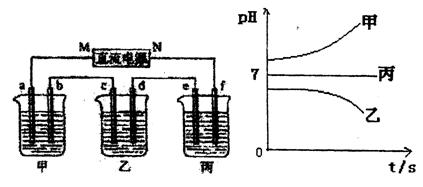
接通电源,经过一段时间后,测得乙中c电极质量增加了16g。常温下各烧杯中溶液的pH与电 解时间t的关系图如上。据此回答下列问题:
解时间t的关系图如上。据此回答下列问题:
(1)M为电源的极(填写“正”或“负”)电极b上发生的电极反应为。
(2)计算电极e上生成的气体在标准状况下的体积;
(3)写出乙烧杯的电解池反应。
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行,为什么?
(5)若经过一段时间后,测得乙中c电极质量增加了16g,要使丙恢复到原来的状态,操作是。
工业上合成甲醇一般采用下列反应: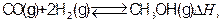 下表是该反应在不同温度下的化学平衡常数(K):
下表是该反应在不同温度下的化学平衡常数(K):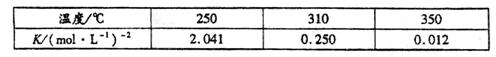
(1)由表中数据判断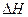 0(填“>”、“=”或“<”)。
0(填“>”、“=”或“<”)。
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol·L-1,则此时的温度为℃。
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表: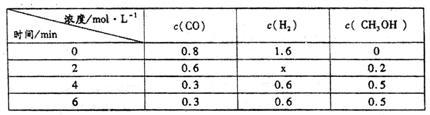
①反应从2min到4min之间,H2的反应速率为。
②反应达到平衡时CO的转化率为。
③反应在第2min时改变了反应条件,改变的条件可能是(填序号)。
a.使用催化剂 b.降低温度 c.增加H2的浓度
(4)常温常压 下:
下:
①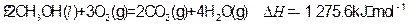
②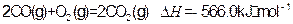
③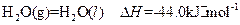
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳。该电池的负极反应式为:。
若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H2体积(标况)为L。
(14分)Ⅰ.反应物与生成物有:浓H2SO4、K2S、K2SO4、SO2、H2O和一种未知物质X。
(1)已知K2S在反应中失去电子,则该反应的氧化剂是。
(2)已知0.5molK2S在反应中失去1mol电子生成X,则X的化学式为。
(3)将氧化剂和还原剂及其配平后系数填入下列空格中,并标出电子转移的方向和数目: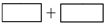
(4)若反应中浓H2SO4过量,则 产物中无X生成,请完成此化学反应方程式:。
产物中无X生成,请完成此化学反应方程式:。
Ⅱ .短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1﹕1的离子化合物A,X与Z能形成原子个数比为1﹕1的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):
.短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1﹕1的离子化合物A,X与Z能形成原子个数比为1﹕1的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):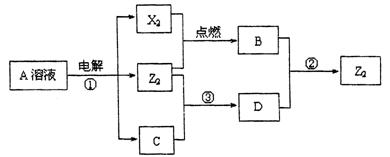
(1)Y在周期表的位置是;
(2)反应①的化学方程式是
 。
。
(3)D溶液呈碱性的原因是(用离子方 程式表示)。
程式表示)。
D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示(夹持固定装置的仪器已略去)。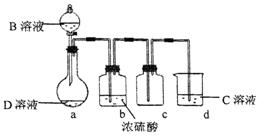
(4)写出反应②的离子方程式。
(5)上述实验装置不够完善,改进方法是。
除去括号中杂质,写出所加试剂与反应的离子方程式。
(1)SO42― (CO32― ),所加试剂:,离子方程式
(2)Cl―― (SO42― ),所加试剂:,离子方程式
(3)Fe2+ (Cu2+),所加试剂:,离子方程式
(4)BaCl2 (HCl ),所加试剂:,离子方程式