超音速飞机在平流层飞行时,尾气中的会破坏臭氧层。科学家正在研究利用催化技术将尾气中的和转变成和,化学方程式如下:

 为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的和浓度如表:
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的和浓度如表:



 请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
 (1)在上述条件下反应能够自发进行,则反应的0(填写">"、"<"、"=")。
(1)在上述条件下反应能够自发进行,则反应的0(填写">"、"<"、"=")。
 (2)前2内的平均反应速率=。
(2)前2内的平均反应速率=。
 (3)在该温度下,反应的平衡常数=。
(3)在该温度下,反应的平衡常数=。
 (4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高转化率的是。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高转化率的是。
| A. |
选用更有效的催化剂 |
| B. |
升高反应体系的温度 |
| C. |
降低反应体系的温度 |
| D. |
缩小容器的体积 |

 (5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。

 ①请在上表格中填入剩余的实验条件数据。
①请在上表格中填入剩余的实验条件数据。
 ②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中浓度随时间变化的趋势曲线图,并标明各条曲线是实验编号。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中浓度随时间变化的趋势曲线图,并标明各条曲线是实验编号。
苄佐卡因(D)是一种医用麻醉药品,它以对硝基甲苯为主要原料经下列反应制得: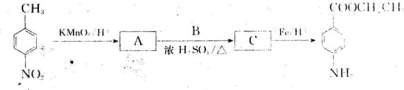
已知,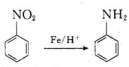
请回答下列问题:
(1)写出A中含氧官 能团的名称。
能团的名称。
(2)写出同时符合下列两项要求的C的一种同分异构体的结构简式:。
①属于1,4—二取代苯,其中苯环上的一个取代基是硝基(—NO2)
②分子中含有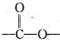 结构的基因,但不显酸性
结构的基因,但不显酸性
(3)写出反应A→C的化学方程式:;该反应属于反应。
(4)苄佐卡因(D)的水解反应如下: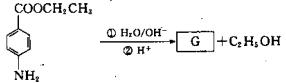
化合物G经缩聚反应可制成高分子纤维,广泛用于通讯、导弹、宇航等领域。则该高分子纤维的结构简式为。
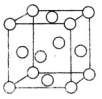 铜合金是人类使用最早的金属材料,铜在化合物中常见的化合价有+1、+2价,能形成多种铜的化合物。
铜合金是人类使用最早的金属材料,铜在化合物中常见的化合价有+1、+2价,能形成多种铜的化合物。
(1)基态铜离子(Cu+)的电子排布式为。
(2)+2价铜可形成化合物[Cu(NH3)4]SO4,下列各项中,该物质
中不含的化学键类型是(填字母序号)。
| A.离子键 | B.金属键 | C.配位键 | D.共价键 |
(3)+1价铜形成的配合物溶液能吸收CO和乙烯(CH2=CH2),
乙烯分子中六个原子在同一平面内,则乙烯分子中C原子
的杂化轨道类型为。
(4)金属铜的晶体类型属于金属晶体,其晶胞结构如右图所示,该晶胞实际拥有个铜原子。
磷肥生产中形成的副产物石膏(CaSO4·2H2O可以转化为硫酸钾肥料和氯化钙水合物储热材料。以下是转化的工艺流程示意图)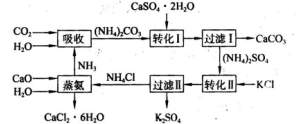
(1)本工艺中所用的原料除CsSO4·2H2O、KCl、H2O和NH3外,还需要等原料。
(2)本工艺中,提高吸收CO2能力的方法是。
(3)工业上用铁做催化剂合成原料气NH3时,常控制温度在700K左右,原因是。
(4)上述工艺流程中体现绿色化学理念的是(写出三条即可)
钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。
已知:SrSO4(s)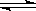 Sr2+(aq)+SO2-4(aq)KSP=
Sr2+(aq)+SO2-4(aq)KSP= 2.5×10-7
2.5×10-7
SrSO3(s)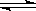 Sr2+(aq)+CO2-4(aq)KSP=2.5×10-9
Sr2+(aq)+CO2-4(aq)KSP=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为,该反应的平衡常数表达式为;该反应能发生的原因是。(用沉淀溶解再平衡的有关理 论解释)
论解释)
(2)对于上述反应,实验证明增大CO2-3的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”、“减小”或“不变”):
①升高温度,平衡常数K将;
②增大CO2-3的浓度,平衡常数K将。
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3。
实验所用试剂为;实验现象及其相应结论。
(4)BaCl2溶液和Ba(NO3)2溶 液是实验中检验SO2-4的常用试剂。某化学研究性学习小组检验某溶液中存在SO2-4时,首先加入Ba(NO3)2溶液,产生白色沉淀,然后加入过量稀硝酸,白色沉淀不溶解,由此得出结论:溶液中一定含有SO2-4。
液是实验中检验SO2-4的常用试剂。某化学研究性学习小组检验某溶液中存在SO2-4时,首先加入Ba(NO3)2溶液,产生白色沉淀,然后加入过量稀硝酸,白色沉淀不溶解,由此得出结论:溶液中一定含有SO2-4。
你认为该推理是否严密?试说明理由。
煤经过化学加工可转化为气体或液体燃料以及各种化工产品,从而提高了煤的利用率。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
C(s)+H2O(g)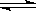 CO(g)+H2(g)△H=131.5kJ·mol-1
CO(g)+H2(g)△H=131.5kJ·mol-1
①下列措施中,不能提高碳的转化率的是(填字母序号)。
a.容器的容积不变,增加水蒸汽的物质的量
b.缩小容器的容积,增大压强
c.及时将水煤气从容器中移走
d.其他条件不变,升高温度
②又知,C(s)+CO2(g)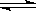 2CO(g)△H=172.5kJ·mol-1
2CO(g)△H=172.5kJ·mol-1
则CO(g)+H2O(g)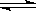 CO2(g)+H2(g)的焓变(△H)为。
CO2(g)+H2(g)的焓变(△H)为。
(2)CO与H2在一定条件下可反应生成甲醇,CO(g)+2H2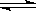 CH3OH(g)。甲醇是一种燃料,可用于设计燃料电池。下图是甲醇燃料电池的原理示意图。
CH3OH(g)。甲醇是一种燃料,可用于设计燃料电池。下图是甲醇燃料电池的原理示意图。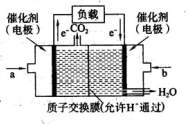 ①a处通入的是(填物质名称),左侧电极上发
①a处通入的是(填物质名称),左侧电极上发
生(填“氧化”或“还原”)反应。
②该电池工作过程中,H+的移动方向为从到
(填“左”或“右”)
③该电池正极反应式为。
④若用该电池提供的电能电解60mL NaCl溶液,设有
0.01molCH3OH完全放电,NaCl足量,且电解产生的
Cl2全部溢出,电解前后忽略溶液体积的变化,则电解结束后所得溶液的pH=。
(3)将等量的CO(g)和H2O(g)分别通入到容积为2L的恒容密闭容器中进行如下反应,
CO(g)+H2O(g) CO2(g)+H2(g)△H=akJ·mol-1,得到下列数据:
CO2(g)+H2(g)△H=akJ·mol-1,得到下列数据: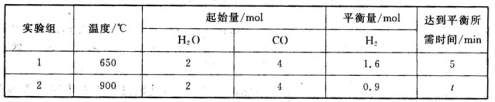
①在实验1中,以v(CO2)表示该反应的反应速率为mol·L-1·min-1;
②在实验2中,t5。(填“>”、“<”或“=”)