已知、和三种元素的原子序数之和等于42。元素原子的4轨道上有3个未成对电子,元素原子的最外层2轨道上有2个未成对电子。跟可形成化合物,元素可以形成负一价离子。请回答下列问题:
已知、和三种元素的原子序数之和等于42。元素原子的4轨道上有3个未成对电子,元素原子的最外层2轨道上有2个未成对电子。跟可形成化合物,元素可以形成负一价离子。请回答下列问题:
 (1)元素原子基态时的电子排布式为,该元素的符号是;
(1)元素原子基态时的电子排布式为,该元素的符号是;
 (2)元素原子的价层电子的轨道表示式为,该元素的名称是;
(2)元素原子的价层电子的轨道表示式为,该元素的名称是;
 (3)与可形成化合物,该化合物的空间构型为;
(3)与可形成化合物,该化合物的空间构型为;
 (4)已知化合物在稀硫酸溶液中可被金属锌还原为,产物还有和,该反应的化学方程式是_;
(4)已知化合物在稀硫酸溶液中可被金属锌还原为,产物还有和,该反应的化学方程式是_;
 (5)比较的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由。
(5)比较的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由。
A、B、C、D、E是中学化学常见的分子或离子,它们核外都有10个电子,且A是由5个原子核组成的粒子。它们之间可发生如下变化:A+B===C+D;B+E===2D,且D与大多数酸性氧化物及碱性氧化物均能反应。
(1)A的电子式:____________B的电子式:____________
(2)E的化学式为:__________
(3)用电子式表示D的形成过程:
(4)实验室制取C的方程式:
向10ml0.1mol/l的Na[Al(OH)4]溶液中滴加0.1mol/l的HCl溶液,生成沉淀的量与加入的盐酸体积的关系如图
(1)写出OA段的离子方程式
(2)写出AB段的化学方程式
(3)OB段反应共消耗ml盐酸溶液;
此过程中生成沉淀最多时,沉淀物质的量是mol,此时消耗的盐酸是ml
(10分)⑴键线式 表示的分子式;名称是。
表示的分子式;名称是。
⑵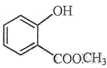 中含有的官能团的名称为
中含有的官能团的名称为
⑶丁基的4个结构简式为________________________________________________________
⑷含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、蒸馏瓶、_______ __、_________、尾接管、锥形瓶
写出支链上共含有3个C原子,主链上含碳原子数最少的烯烃的结构简式。
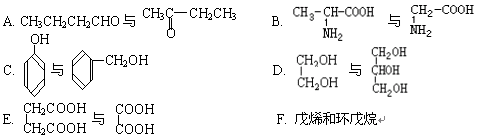
下列各化合物中,属于同系物的是,属于同分异构体的是(填入编号)