A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。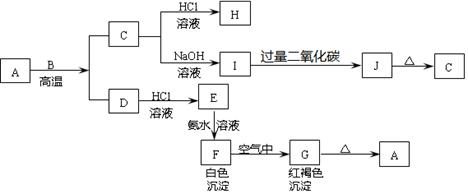
(1)写出下列物质的化学式:
A: E: J: G:
(2)按要求写方程式:
①A与B生成C和D的化学方程式: 。
②F在空气中转化为G的化学方程式: 。
③I转化为J的离子方程式: 。
现有NH4Cl和NH3·H2O组成的混合溶液,若其pH=7,则该溶液中c(NH4+)___c(Cl-);若pH>7,则该溶液中c(NH4+)______c(Cl-)。(填“>”、“<”、“=”).
现有以下物质:①NaCl晶体;②液态SO3;③纯醋酸;④汞;⑤BaSO4固体;⑥纯蔗糖;⑦酒精;⑧熔化的KNO3;请回答下列问题:
(1)以上物质能导电的是;(2)以上物质属于电解质的是;
(3)以上物质属于非电解质的是;以上物质中溶于水后形成的溶液能导电的是。
(6分)按要求写出相应的方程式:电离方程式:
(1)H2S:____________________________。
(2)NH4HSO4____________________________。
水解反应的离子方程式:
(1)CuSO4____________________________。
(2)Na2CO3____________________________。
(3)AlCl3+Na2S____________________________。
浓度均为0.1mol/L的8种溶液:①HNO3②H2SO4③CH3COOH④Ba(OH)2⑤NaOH⑥CH3COONa⑦KCl⑧NH4Cl其溶液的pH由小到大的顺序是 。
有5 种 短周期元素的原子序数按E、D、B、A、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合
短周期元素的原子序数按E、D、B、A、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合 物A2B,A2B中所有粒子的电子数相同,且电子总数为30;D和E可形成4核10电子的分子。试回答下列
物A2B,A2B中所有粒子的电子数相同,且电子总数为30;D和E可形成4核10电子的分子。试回答下列 问题:
问题:
(1)写出五种元素的名称:ABCDE。
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出下列物质的电子式:
D元素形成的单质;B与E形成的化合物;
A、B、E 形成的化合物;D、E形成的化合物
形成的化合物;D、E形成的化合物