在下列溶液中,各组离子一定能够大量共存的是
A.pH=2的溶液: Fe3+、Cu2+、SO42-、NO3- |
B.c(H+)=1×10-12mol/L的溶液:NH4+、K+、Cl-、AlO2- |
C.水电离的c(H+)=1×10-12mol/L的溶液:Na+、Al3+、Br-、ClO-  |
D.与铝反应放出氢气的溶液:Na+、Mg2+、Br-、Cl- |
下列解释实验事实的离子方程式正确的是
| A.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
| B.漂白粉溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3- |
| C.酸性KI淀粉溶液久置后变蓝:4l-+O2+4H+=2I2+2H2O |
D.Na2S溶液使酚酞试液变红:S2-+2H2O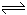 2OH-+H2S 2OH-+H2S |
下列有关溶液的说法中,正确的是
| A.物质的量浓度相等的NH4Al(SO4)2、NH4HCO3、NH4Cl溶液中c(NH4+):NH4HCO3>NH4Cl>NH4Al(SO4) 2 |
| B.1.0mol/L Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C.测得酸式盐NaHA溶液的pH=3,则NaHA在溶液中一定是电离大于水解 |
D.常温下0.4 mol/L HB溶液与0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c (Na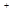 )> c (B )> c (B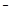 )> c (H )> c (H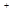 )> c (OH )> c (OH ) ) |
用下列实验装置进行相应的实验,能达到实验目的的是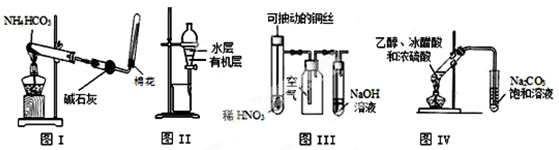
| A.图I所示装置用于制取少量的氨气 |
| B.图II所示装置用于提取I2的CCl4溶液中的I2 |
| C.图III所示装置微热稀HNO3,在广口瓶中可收集NO气体 |
| D.图IV所示装置可制取少量的乙酸乙酯 (夹持物略) |
下列有关因果关系的描述正确的是
| A.因为盐酸的酸性强于氢硫酸,所以氯元素的非金属性强于硫 |
| B.因为醋酸电离吸热,所以用NaOH溶液恰好中和等体积等浓度的醋酸和盐酸,前者放出热量少 |
C.钠的金属性比钾强,工业上用钠制取钾(Na+KCl K↑+NaCl) K↑+NaCl) |
| D.因为某吸热反应能自发进行,所以该反应是熵减反应 |
抗禽流感药物达菲可用莽草酸为原料合成,其结构简式如图,下列关于莽草酸的说法正确的是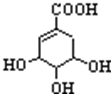
| A.分子式为C7H6O5 |
| B.分子中含有2种官能团 |
| C.可发生加成和取代反应 |
| D.莽草酸遇FeCl3溶液会呈现特征颜色 |