合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
① CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
② CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
③ CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
⑴ 在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。反应进行的前5 min内, v(H2)= ▲ ;10 min时,改变的外界条件可能是 ▲ 。
|


| CO |
H2O |
CO2 |
H2 |
| 0.5 mol |
8.5 mol |
2.0 mol |
2.0 mol |
此时反应③中正、逆反应速率的关系式是 ▲ (填代号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
(1)表中最活泼的金属与最活泼的非金属形成的化学式是_______,含有(填离子键、共价键)
(2)⑦号元素的原子结构示意图为___________,其单质既能与酸反应,又能与碱反应,写出与碱反应的化学方程式。_________________________________________。
(3)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是(写化学式),
④、⑤、⑧氢化物稳定性由强到弱的顺序是(写化学式)。
(4)①、④、⑥三种元素形成的化合物中化学键的类型:。其化合物类型为
。(填共价化合物、离子化合物)
(5)②和④形成的化合物与④和⑥形成的化合物之间发生氧化还原反应,写出该反应的
化学方程式:。
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
1)写出并配平CCl4层由紫色变成无色的化学反应方程式。
2)整个过程中的还原剂是。
3)把KI换成KBr,则CCl4层变为__色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是。
4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若庄Kl与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
.在下图转化关系中,固体甲的焰色反应呈黄色,M为常见的液体物质,I为常见金属,且I与G的稀溶液不反应,只能与G的浓溶液在加热条件下反应;酸G是重要的化工产品和化工原料;H为良好的耐火材料(图中部分产物没有列出)。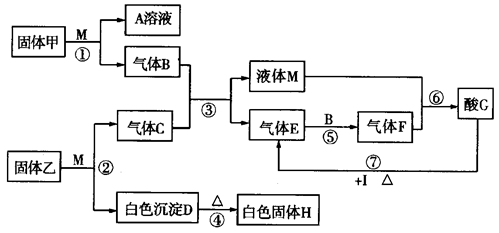
(1)固体甲的名称为__________,F的化学式为______________。
(2)反应①~⑦中属于氧化还原反应的是______________(填写反应序号)。
(3)工业废气中常含有气体E,为了充分利用资源、保护环境,目前应用最广泛的工业废气处理方法是石灰法。以生石灰为原料在吸收装置中与气体E反应的化学方程式为:
___________________________________________。
(4)反应⑦的化学反应方程式为_____________________________________________。
(5)已知工业上电解熔融的H冶炼金属单质X,向40.0g固体混合物中(仅含H、Fe2O3、SiO2),加入足量稀盐酸,分离得到12.0g固体;滤液中加入过量A溶液,分离得到21.4g固体;则此混合物中元素X的质量分数为__________________。
某学校研究性学习小组利用实验室常用试剂,
探究硝酸的氧化性。请完成下面的空白:
(1)在具支试管底部滴入5滴浓硝酸,然后用硫化亚铁与盐酸反应制备H2S气体,如图所示通入具支试管中,可以观察到在试管内形成黄烟,黄烟附着在试管内壁上,形成“黄霜”。
出上述制备H2S的离子方程式
______________________________________。
②在试管内壁上的“黄霜”的成分是_______________,该反应说明浓硝酸有氧化性外,实验现象还说明了浓硝酸具有________性。该实验中烧杯内的氢氧化钠溶液的作用是
__________________________________________________________________。
(2)卤族元素单质也具有氧化性,该小组设计了下面的实验探究碘单质与稀硝酸氧化性强弱比较:
①提出合理的假设
假设l:碘单质氧化性强于稀硝酸;假设2:碘单质氧化性弱于稀硝酸。
②设计实验方案,进行实验探究,请写出实验步骤和预期的现象与结论。限选实验试剂与仪器:稀硝酸、KI溶液、四氯化碳;试管、胶头滴管。
X、Y、Z、M、N为原子序数小于18的五种元素,X原子的电子层数等于最外层电子数;X与Y处于同一周期,Y与M可形成离子化合物M2Y,该化合物的水溶液显碱性;Z离子核内质子数与核外电子数之和为18;X、Z、M三种元素的离子具有相同的电子层排布;元素N的原子的质子、中子与电子数之和为2。
根据上述信息回答下列问题:
(1)写出质量数为32的Y原子符号____________,M2Y的电子式为________________。
(2)X、Z、M三种元素的离子半径大小顺序为_________________(用离子符号表示)。
(3)下列说法中正确的是___________________________。
| A.元素Z与元素M形成的化合物中只有极性共价键和离子键 |
| B.元素M和元素N之间不能形成离子化合物 |
| C.元素X的原子比元素M的原子的失电子能力强 |
| D.元素Z与元素N形成的简单化合物比元素Y与元素N形成的化合物稳定 |
(4)写出X、M两元素的最高价氧化物对应的水化物反应的离子方程式:
__________________________________________________________________________。
(5)已知(4)反应中生成的含X元素的化合物与HF、NaCl按l :6 :2的物质的量之比恰好完全反应,得到H2O、HCl和另一种含有三种元素且微溶于水的化合物,写出该反应的化学方程式__________________________________________________________。