⑴中学化学教材中图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g/mol)。








⑵天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某氧化镍晶体中就存在如图4-4所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。
有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液进行下列实验。
| 实验步骤 |
实验现象 |
| ①取少量该溶液,加几滴甲基橙 |
溶液变红色 |
| ②取少量该溶液加热浓缩,加铜片和浓硫酸加热 |
有无色气体产生,气体遇空气可以变成红棕色 |
| ③取少量该溶液,加BaCl2溶液 |
有白色沉淀生成 |
| ④取③中上层清液,加AgNO3溶液 |
有白色沉淀生成,且不溶于稀硝酸 |
| ⑤取少量该溶液,加NaOH溶液 |
有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定存在的离子是________________,溶液中肯定不存在的离子是________________。
(2)为进一步确定其他离子,应该补充的实验及对应欲检验离子的名称(说明使用试剂的名称,不必写详细操作步骤)是____________________________。
从某些植物树叶中提取的挥发油含有下列主要成分: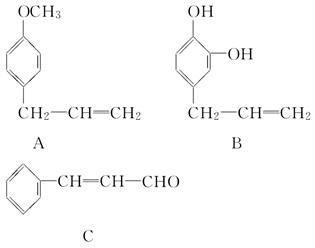
(1)写出A物质可能发生的反应类型(至少三种)__________________________。
(2)1 mol B与足量的溴水充分反应,需消耗________ mol单质溴。
(3)写出C在一定条件下与足量H2反应的化学方程式:
________________________________________________________________________。
(4)已知RCH===CHR′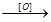 RCOOH+R′COOH。写出C在强氧化剂条件下生成的有机化合物的结构简式:
RCOOH+R′COOH。写出C在强氧化剂条件下生成的有机化合物的结构简式:
________________________________________________________________________。
(5)写出A与B在一定条件下,生成一种高分子化合物的化学方程式:
________________________________________________________________________。
苯酚是重要的化工原料,通过下列流程可合成阿司匹林、香料和一些高分子化合物。已知: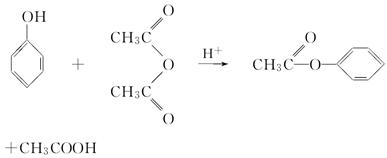
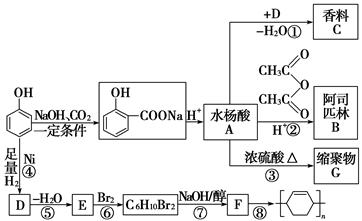
(1)写出C的结构简式:
________________________________________________________________________
________________________________________________________________________。
(2)写出反应②的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(3)写出G的结构简式:
________________________________________________________________________
________________________________________________________________________。
(4)写出反应⑧的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(5)写出反应类型:
④________________________________________________________________________,
⑦__________________________________。
(6)下列可检验阿司匹林样品中混有水杨酸的试剂是________。
a.三氯化铁溶液 b.碳酸氢钠溶液 c.石蕊溶液
下列结构简式中,Ⅰ是扑热息痛,Ⅱ是阿司匹林,它们都是临床应用广泛的解热镇痛药,但Ⅰ易导致肾脏毒性,Ⅱ对胃黏膜有刺激性,多用会引起胃溃疡。Ⅲ是扑炎痛,它是根据药的合成中称为“拼合原理”的手段设计并合成出的解热镇痛药。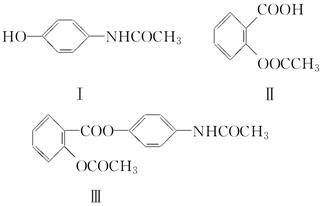
(1)为什么阿司匹林会有上述的副作用?
________________________________________________________________________。
(2)合成扑炎痛反应的反应类型为
________________________________________________________________________。
(3)扑炎痛本身并无解热镇痛效能,但口服后人体内会产生上述药理作用,且毒副作用没有Ⅰ和Ⅱ那么明显,其原因是
________________________________________________________________________
________________________________________________________________________。
以苯为主要原料,可以通过如图所示途径制取阿司匹林和冬青油。请按要求回答: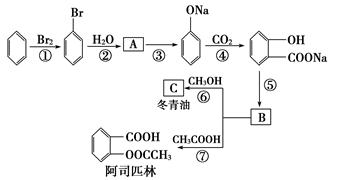
(1)请写出有机物的结构简式:
A______________________;B____________________;
C____________________。
(2)写出变化过程中①、⑥的化学方程式:
反应①________________________________________________________________________;
反应⑥________________________________________________________________________。
(3)变化过程中的②属于________反应,⑦属于________反应。
(4)物质的量相等的冬青油和阿司匹林完全燃烧时消耗氧气的量,冬青油比阿司匹林________。