(8分)在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸, 所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示。
问:
(1)此溶液中同时含有____mol___ 离子;
(2)用离子方程式表示MN段发生的反应是
(3)C(或M)点的纵坐标为0.78,则c(AlO2-)=
(4)点B的横坐标为30,则到点N处滴入的HCl溶液体积为 mL
某无色透明溶液,投入金属铝可放出H2。现有下列离子:Mg2+、Cu2+、H+、Cl-、K+、OH-、CO32-,试判断下列两种情况下,各离子存在于此溶液中的情况:
(1)第一种情况:该溶液中滴加紫色石蕊后呈红色,则该溶液中一定有离子,一定没有离子,可能有离子;
(2)第一种情况:该溶液中滴加紫色石蕊后呈蓝色,则该溶液中一定有离子,一定没有离子,可能有离子。
(16分) 某校化学兴趣小组的同学经查阅资料得知:铝表面致密的氧化膜能使铝与其周围的介质(空气、水等)隔绝,但奇怪的是铝制容器仍不能用来盛放和腌制咸菜。为此该小组的同学对铝表面的氧化膜进行了探究,其过程如下,请完成下列填空。
(1)用坩埚钳夹住一块擦去氧化膜的铝片,放在酒精灯火焰上灼烧,铝片表面接触火焰的部分变暗,片刻后变软,轻轻摇动,会左右摇晃,却不像蜡烛那样滴落。这是因为铝表面氧化膜的熔点________(填“高于”或“低于”)内层铝的熔点,并将其裹住,所以不易发生滴落现象。
(2)取纯净的铝箔,包裹住一小块金属钠后放入水中无现象;将该铝箔用针刺些小孔后再包裹住一小块金属钠后放入水中,迅速就有大量的气泡产生。试解释其中的原因,并写出相关的化学方程式:___________ ___________________。
(3)用砂纸打磨一铝片,使其表面变粗糙,再将其放入CuSO4稀溶液中,2~3 min后有少量红色固体附着在其表面。试写出产生红色固体的离子方程式:。
(4)把两块未用砂纸打磨过的铝片都浸入氢氧化钠溶液中,片刻后其表面产生无色气体。试写出铝的氧化膜与氢氧化钠溶液反应的离子方程式:___________________________。
(5)另取一铝制易拉罐,收集满一罐CO2,加入过量的浓氢氧化钠溶液,立即把口封闭。可以发现易拉罐“咔咔”作响,并变瘪了;过一会后,易拉罐又会作响并鼓起来。试解释为什么,写出有关的离子方程式
运用所学知识,完成下列空白处内容。
(1)取23g钠、24g镁、27g铝分别与足量稀盐酸反应,在相同条件下,产生氢气的体积之比是。
(2)能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是(选填下列字母)。
| A.分别加热这两种固体物质,并将生成的气体通入澄清的石灰水中 |
| B.分别在这两种物质的溶液中,加入CaCl2溶液 |
| C.分别在这两种溶液中,加入同浓度的稀盐酸 |
| D.分别在这两种物质的溶液中,加入少量澄清的石灰水 |
(3)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为,需要二者的固体质量之比为。
(1)在298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水放出热量1558.3 kJ。写出该反应的热化学方程式。
(2)利用该反应设计一个燃料电池:用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入乙烷和氧气。通入乙烷气体的电极应为极(填写“正”“负”)该电极上发生的电极反应式是。
(3)右图所示实验装置中,石墨棒上的电极反应式为;如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 __________(填物质名称)。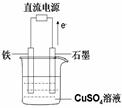
自2010年8月7日,甘肃省舟曲县发生特大泥石流后,各地的救援物资远远不断运往灾区。下图为地方捐助的一种国家准字号补铁补血用药——复方硫酸亚铁叶酸片,其主要成分是绿矾——硫酸亚铁晶体(FeSO4·7H2O)。
Ⅰ、某校课外活动小组为测定该补血剂中铁元素的含量特设计实验步骤如下:
请回答下列问题:
(1)步骤②中加入过量H2O2的目的是。
(2)步骤③中反应的离子方程式为。
(3)步骤④中一系列处理的操作步骤是:过滤、、灼烧、、称量。
(4)若实验无损耗,则每片补血剂含铁元素的质量为g(用含a的代数式表示)。
Ⅱ、灾难过后,灾区的饮用水变得非常的浑浊,不能饮用。因此对污染的饮用水的处理成了非常重要的事,其中处理的方法有很多:
(1)可以用适量绿矾和氯气一起作用于污染的自来水,而起到较好的净水效果;理由是(用离子方程式表示);;。
(2)在使用过程中发现绿矾和氯气的混合使用对酸性废水中的悬浮物处理效果较差,其原因是。