将用于2008年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成聚全氟乙丙烯。下列说法错误的是( )。
| A.ETFE分子中可能存在“—CH2—CH2—CF2—CF2—”的连接方式 |
| B.合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应 |
| C.聚全氟乙丙烯分子的结构简式可能为[ CF2—CF2—CF2—CF-]nCF3 |
| D.四氟乙烯分子中即含有极性键又含有非极性键 |
下列关于元素及其化合物的说法正确的是
| A.Fe在常温下可与浓硝酸、稀硝酸、浓硫酸剧烈反应 |
| B.Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用相同 |
| C.Na久置于空气中,可以和空气中的有关物质发生反应,最终生成Na2CO3 |
| D.制备FeCl3、CuCl2固体均可采用将溶液直接蒸干的方法 |
钠铝合金(常温液态)可作为核反应堆的载热介质。下列说法错误的是
| A.该合金的熔点低于金属钠的熔点 |
| B.若将钠铝合金投入水中得到无色溶液且无固体剩余,则n(Na)≥n(Al) |
| C.若将钠铝合金投入FeCl3溶液中有Fe(OH)3沉淀生成 |
| D.等质量的钠铝合金中铝的含量越大,与足量盐酸反应时放出的氢气越少 |
用下列装置不能达到有关实验目的的是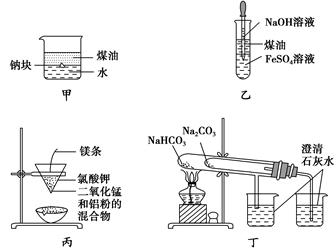
| A.用甲图装置证明ρ(煤油)<ρ(钠)<ρ(水) |
| B.用乙图装置制备Fe(OH)2 |
| C.用丙图装置制取金属锰 |
| D.用丁图装置比较NaHCO3和Na2CO3的热稳定性 |
下列说法在一定条件下可以实现的是
①酸性氧化物与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③没有水生成,也没有沉淀和气体生成的复分解反应
④两种酸溶液充分反应后的溶液体系为中性
⑤有单质参加的非氧化还原反应
⑥两种氧化物反应的产物有气体
| A.①②③④⑤⑥ | B.②④⑤⑥ |
| C.①②③⑤ | D.③④⑤⑥ |
下列相关离子方程式书写正确的是
| A.NaClO溶液与FeCl2溶液混合:6Fe2++3ClO-+3H2O===2Fe(OH)3↓+3Cl-+4Fe3+ |
| B.用食醋检验牙膏中的碳酸钙:CaCO3+2H+===Ca2++CO2↑+H2O |
| C.FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2===2Fe3++2H2O |
D.电解MgCl2水溶液的离子方程式:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |