设NA代表阿伏加德罗常数(NA)的数值,下列说法正确的是
| A.22.4 L Cl2中含有NA个C12分子 |
| B.1 L 0.1 mol·L-1 Na2SO4溶液中有0.1 NA个Na+ |
| C.1 mol H2与1 mol C12反应生成NA个HCl分子 |
| D.1 mol Ca变成Ca2+时失去的电子数为2NA |
下列除杂所用试剂和操作不合理的是
| 选项 |
物质(括号中为杂质) |
除杂试剂 |
操作 |
| A |
CO2(SO2) |
饱和NaHCO3溶液 |
洗气 |
| B |
BaCO3(BaSO4) |
饱和Na2CO3溶液 |
搅拌、过滤 |
| C |
苯(苯酚) |
浓溴水 |
过滤 |
| D |
Cl2(HCl) |
饱和食盐水 |
洗气 |
装置图所示, 有关分析不正确的是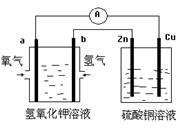
| A.该装置中Cu极为阳极 |
| B.工作时,左池中K+移向a电极 |
| C.工作一段时间,要使右池溶液复原可加入适量的CuO |
| D.b极的电极反应式:H2+2OH--2e-= 2H2O |
下列描述及热化学方程式均正确的是
| A.已知C2H6的燃烧热为1090 kJ·mol-1,则C2H6燃烧的热化学方程式为: C2H6(g)+3.5O2(g)===2CO2(g)+3H2O(g)ΔH=-1090 kJ/mol |
| B.25℃,101kPa下,l mol C6H6燃烧生成CO2和液态水时放出3260 kJ热量,其热化学方程式为:C6H6(g)+7.5O2 (g)=6CO2 (g)+3H2O (l)△H=-3260kJ•mol-1 |
| C.已知常温下:H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3 kJ/mol,则稀醋酸与稀NaOH溶液反应生成1 mol H2O(l)时也放出57.3 kJ的热量 |
| D.已知2CO(g)+O2(g)===2CO2(g)ΔH=-566 kJ·mol-1,则CO的燃烧热ΔH=-283 kJ·mol-1 |
下列电解质溶液中微粒的物质的量浓度关系一定正确的是
| A.在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B.在0.1 mol·L-1NaClO溶液中:c(OH-)=c(H+)+ c(HClO) |
| C.某温度下,CH3COOH溶液中滴入NaOH溶液,使溶液pH=7时:c(CH3COO-)=c(Na+)> c(H+)=c(OH-) |
| D.已知酸性:HCOOH>CH3COOH,相同浓度的HCOOK与CH3COONa溶液中C(K+)-c(HCOO-)>c(Na+)-c(CH3COO-)[ |
下列表示对应化学反应的离子方程式.其中正确的是
| A.向NaAlO2溶液中通入过量的CO2:2AlO2﹣+CO2+3H2O═2Al(OH)3↓+CO32﹣ |
| B.NH4HCO3溶液中加入过量氢氧化钠溶液:NH4++OH﹣═ NH3.H2O |
| C.AlCl3溶液中滴加过量氨水:Al3+ + 3NH3.H2O ═ 3NH4++ Al(OH)3↓ |
| D.磁性氧化铁(Fe3O4)溶于稀硝酸3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O |