有一工业烧碱(含氯化钠),现要求采用学过的定量实验的方法测定此工业烧碱中氢氧化钠的质量分数(假设各步实验中试样的损失忽略不计),请完成如下实验报告。
实验报告
(一) 实验目的:工业烧碱中氢氧化钠的质量分数测定
(二) 实验原理:(写出有关离子反应方程式):_____________________________,
(三) 实验试剂:工业烧碱、标准浓度的盐酸、甲基橙。
(四) 实验仪器:铁架台(成套)、天平、烧杯、锥形瓶、移液管、胶头滴管、100ml量筒、 ________、_______。
(五) 按实验顺序填写实验步骤:(中和滴定法)
______、溶解、移液管量取一定体积的待测液于洁净的锥形瓶中、__________、用标准盐酸滴定至终点。
当滴定至溶液由______色变为_____色,且半分钟不腿色时停止滴定。在相同条件下重复二次。
(六)数据处理及问题讨论:
1、若要测定样品中氢氧化钠的质量分数,实验中至少需要测定那些实验数据?_______________________________________。
2、取a克样品,配置100mL溶液,取20mL待测液,用C mol/L的标准盐酸滴定至终点,消耗盐酸VmL。试写出样品中氢氧化钠的质量分数表达式为: 。
某研究小组在实验室中将工厂废弃的合金,经过一系列的反应,制得氯化铝固体、硝酸铜晶体和铁红。其实验方案如下:
(1)该小组所用的合金中含有的金属为铁、 、 (填名称)。
(2)操作①、③使用的主要玻璃仪器是_,简述操作②的方法: 。操作④实验操作步骤包括:加热浓缩、冷却结晶、 (填操作名称)、洗涤、干燥。
(3)写出滤渣B中较活泼金属与足量稀HN03后发生反应的离子方程式: ;
(4)若该小组通过上述实验流程制得铁红80g,假设实验过程中无质量损失,则合金中铁的质量为 g;
(5)上述实验流程中符合“绿色化学”理念的做法是 (答出一点即可)。
(1)某工厂用NH3和空气来联合处理工厂尾气中的等体积SO2和NO2,不仅除去了有害气体,还得到副产品—含两种按盐的化肥。若反应所消耗的NH3和空气的体积比为4:5(空气中O2的体积分数以 计),则处理废气时发生反应的总化学方程式为 。若该工厂用此方法处理废气,一天中消耗了空气336m3(假定反应中O2无损失),则生成化肥的总质量为 。
计),则处理废气时发生反应的总化学方程式为 。若该工厂用此方法处理废气,一天中消耗了空气336m3(假定反应中O2无损失),则生成化肥的总质量为 。
(2)该工厂废气中含有大量温室气体—CO2。为减少碳排放,该工厂尝试用以下反应制备甲醇: 。一定温度下,在恒容的密闭容器中充入1 mol CO2和3mol H2。实验测得CO2和CH3 OH (g)的浓度随时间变化如下图所示。
。一定温度下,在恒容的密闭容器中充入1 mol CO2和3mol H2。实验测得CO2和CH3 OH (g)的浓度随时间变化如下图所示。
0-10分钟内,CH3 OH的生成速率为 ,达平衡时,CO2转化率为 ,若第 10min时,向容器中再通人3mol H2,再次达平衡时,CO2的转化率会 (填“增大”、“减小”或“不变”)。
(本题共14分)丙烯是重要的工业原料,以丙烯为原料合成有机玻璃和药物喹啉的流程如下: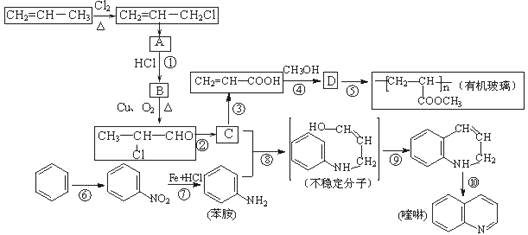
结构简式:A为 , C为 ;
①~⑩反应中属于属于消去反应的有 ;
设计反应①、②的目的是 ;
反应①的方程式为 ;
反应④的方程式为 ;
反应⑦的化学反应类型是 ;
反应②的条件为 。
(本题共8分)二氧化碳和氢气在一定条件下可以制得烯烃,该技术已成为节能减碳的有效途径之一。已知二氧化碳和氢气按1:3比例可合成烯烃B, B的产量是衡量一个国家石油化工水平的标志。下图是合成橡胶和TNT的路线。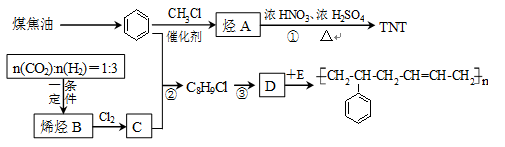
已知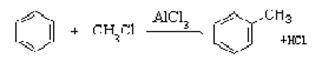
工业上由煤焦油提取苯的操作名称为_______。E的结构简式为__________________。
写出反应类型:反应②________________;反应③__________________。
写出反应D+E的化学方程式_______________________。
D在一定条件下与足量H2反应后的产物,其一氯代物有_________种。
(本题共16分)碳纳米管是近年来发展迅速的一种具有特殊结构及优异性能的纳米材料。它是由碳原子形成的无缝、中空管体材料,主要由五边形、六边形的碳环组成,相当于石墨结构卷曲而成,结构如下。
写出一种与碳纳米管互为同素异形体物质____________。
储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:
C + K2Cr2O7 + H2SO4→ CO2 + K2SO4 + Cr2(SO4)3 + H2O
配平上述化学方程式并标出电子转移方向与数目;此反应的被还原的元素是 ,氧化产物是 ;
H2SO4在上述反应中表现出来的性质是 (填选项编号)
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
上述反应若产生0.1mol CO2气体,则转移电子的物质的量是 mol。
NaNO2有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。下列说法正确的是 (填序号)。
| A.解毒剂美蓝应该具有氧化性 | B.中毒时亚硝酸盐发生氧化反应 |
| C.解毒时高铁血红蛋白被还原 | D.中毒过程中血红蛋白显氧化性 |
已知NaNO2能发生如下反应:NaNO2+HI →NO+I2+NaI+H2O (未配平), 从上述反应推知 (填序号)。
| A.氧化性:I2>NaNO2 | B.氧化性:NaNO2>I2 |
| C.还原性:HI>NO | D.还原性:I2>HI |
根据上述反应,可用试纸和生活中常见的物质进行实验来鉴别NaNO2和NaCl。现供选用的物质有:①白酒 ②碘化钾淀粉试纸 ③淀粉 ④白糖 ⑤食醋,进行本实验时,可以选用的物质至少有 (填序号)。
某工厂的废液中含有2%~5%的NaNO2,直接排放会造成污染。下列试剂中:①NaCl ② NH4Cl ③HNO3④浓H2SO4,能使NaNO2转化为N2的是 (填序号)。