你认为减少酸雨产生的途径可采取的措施是
①用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
| A.①②③ | B.②③④⑤ |
| C.③⑤ | D.①③④⑤ |
将4 mol A和2 mol B放入2 L密闭容器中发生反应:2A (g)+B(g)2C(g);ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是()
A.4 s内,v(B)=0.075 mol/(L·s)
B.4 s后平衡状态下,c(A)∶c(C)=2∶1
C.达到平衡状态时,若只升高温度,则C的物质的量浓度增大
D.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)  SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是()
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是()
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是()
C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是()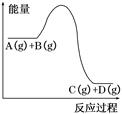
| A.该反应的正反应为放热反应 |
| B.升高温度,利于A的转化率增大 |
| C.加入催化剂时,该反应的反应热发生改变 |
| D.增大压强,能够加快反应达到平衡状态的速率 |
由丙烯合成正丁醛的反应:CH3CH=CH2(g)+CO+H2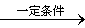 CH3CH2CH2CHO(l)
CH3CH2CH2CHO(l)
该反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是()
| A.低温、高压、催化剂 |
| B.适当的温度、高压、催化剂 |
| C.常温、常压、催化剂 |
| D.适当的温度、常压、催化剂 |
一定条件下的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH=-905.9 kJ/mol,下列叙述正确的是()
4NO(g)+6H2O(g)ΔH=-905.9 kJ/mol,下列叙述正确的是()
| A.4 mol NH3和5 mol O2反应,达到平衡时放出的热量为905.9 kJ |
B.平衡时v正(O2)=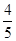 v逆(NO) v逆(NO) |
| C.平衡后降低压强,混合气体平均摩尔质量增大 |
| D.平衡后升高温度,混合气体中NO含量降低 |