2007 年诺贝尔化学奖授予德国化学家 GerhardErtl ,以表彰他对固体表面化学过程研究的重大发现。使 CO、NOx等在铂表面发生化学反应转变成无毒气体,以减少汽车尾气中有毒气体的排放,正是此项研究的重要应用之一。下列有关说法不正确的是
| A.CO在铂表面被氧化生成CO2 | B.汽车尾气中NOx在铂表面反应转化为N2 |
| C.CO在铂表面可与O2、NOx反应 | D.铂在反应中起氧化作用 |
下列各反应属于原电池反应的是
| A.氧化铝膜破坏后,金属铝被迅速氧化 |
| B.锌与稀硫酸反应中加入少量CuSO4溶液,反应放出H2的速率加快 |
| C.红热的铁与水接触表面上形成蓝黑色的保护层 |
| D.铁丝在氯气中燃烧产生大量棕黄色的烟 |
设C+CO2 2CO(正反应吸热),正反应的反应速率为v1;N2+3H2
2CO(正反应吸热),正反应的反应速率为v1;N2+3H2 2NH3(正反应放热),正反应的反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为
2NH3(正反应放热),正反应的反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为
| A.同时增大 | B.同时减小 |
| C.v1增大,v2减小 | D.v1减小,v2增大 |
下列有关燃料电池的说法正确的是
| A.氢氧燃料电池可将热能直接转变为电能 |
| B.燃料电池的能量转化率可达100% |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.以KOH溶液为电解质溶液的氢氧燃料电池,负极反应为O2 + 2H2O + 4e- =4OH- |
在N2+3H2 2NH3的反应中,在5s中N2由6mol/L减至2mol/L。则NH3的平均反应速率是
2NH3的反应中,在5s中N2由6mol/L减至2mol/L。则NH3的平均反应速率是
| A.2.4 mol/(L·s) | B.1.6mol/(L·s) |
| C.0.8 mol/(L·s) | D.0.08 mol/(L·s) |
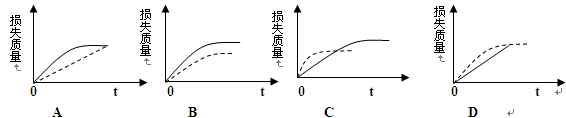
将ag块状碳酸钙跟足量的盐酸反应,反应物损失的质量随时间的变化曲线如图中的实线所示,在相同条件下,将bg(a>b)粉末状碳酸钙与同浓度的盐酸反应,则相应的曲线如图中的虚线所示。其中正确的是