现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
能形成双原子分子,原子间存在3对共用电子对 |
| X |
M层有3个电子 |
| Y |
最外层电子数是最内层电子数2倍,其最高氧化物是一种固体,用于生产光导纤维 |
| Z |
最高正价为+7价 |
(1)写出元素Z的离子结构示意图 ▲ 。
Y的最高价氧化物中,化学键Y—O的物质的量与Y的物质的量之比为: ▲(填数字)。
(2)X的最高价氧化物与烧碱反应的离子反应方程式为: ▲ 。
(3)Z的非金属性比T元素强,用化学方程式表示: ▲ 。
(4)XT是一种新型的无机材料,可由X的最高价氧化物与T的单质及焦炭反应生成,逸出的气体具有可燃性,写出反应方程式,并标出电子转移方向和数目。
▲ 。
A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为;
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为,C的元素符号为;
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为,其基态原子的电子排布式为。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为,其基态原子的电子排布式为。
某无色溶液,由Na+、Ag+、Ba2+、Al3+、、、中的若干种组成。取该溶液进行如下实验:
(A)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
(B)在(A)所得溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
(C)在(B)所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。根据上述实验回答下列问题:
⑴溶液中一定不存在的离子是。
⑵一定存在的离子是。
⑶请你写出判断沉淀乙成份的方法和步骤是
(8分)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。
已知该反应中H2O2只发生如下过程:H2O2 → O2
(1)写出该反应的化学方程式,并标出电子转移的方向和数目。
(2)该反应中的氧化剂是。
(3)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为。
仔细体会下列有机合成过程中碳骨架的构建及官能团的引入和转化,完成下题:
已知两个醛分子在NaOH溶液作用下可以发生加成反应,生成一种羟基醛: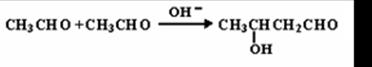
肉桂醛F(分子式为C9H8O)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的: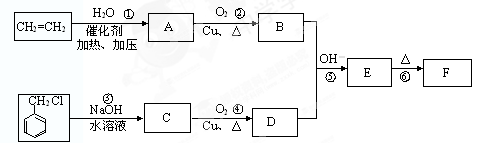
已知:反应⑤为羟醛缩合反应。请回答:
(1)肉桂醛F的结构简式为:。E中含氧官能团的名称为。
(2)反应①~⑥中符合原子经济性的是。
(3)写出下列转化的化学方程式:
②,③。
写出有关反应的类型:②⑥。
(4)符合下列要求的E物质的同分异构体有种(苯环上有两个取代基,其中有一个甲基在对位且属于酯类)。
将饱和FeCl3溶液滴入沸水中,液体变为________色,得到的是_________。
用此分散系进行下列实验:
(1)将其装入U型管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色________,这说明________________,这种现象称为__________。
(2)向其中加入饱和(NH4)2SO4溶液发生的现象是______,原因是_________。
(3)向其中滴入过量稀硫酸,现象是______________,其原因是_________________。
(4)提纯此分散系常用的方法是________。