黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
 (2)上述冶炼过程中产生大量SO2。下列处理方案合理的是 (填代号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是 (填代号)。
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3
d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:
S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程。 、 (不必配平)。
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、AI2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 。证明炉渣中含有的实验现象为
。
聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛应用于制作光导纤维。已知A为某种聚甲基丙烯酸酯纤维的单体,其转化关系如下: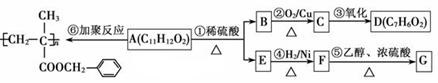
(1)A的结构简式为 。
(2)下列有关E的说法不正确的是 (填写字母编号)
| A.能使酸性高锰酸钾溶液褪色 | B.能使溴的CCl4溶液褪色 |
| C.一定条件下,能够发生消去反应 | D.一定条件下,能够发生取代反应 |
(3)F的同分异构体中属于酯类的有 种
(4)反应②的化学方程式是
反应⑤的化学方程式是
按要求完成下列问题:
(1) 系统命名为 ;
系统命名为 ;
(2)4―甲基―1―戊烯的键线式为 。
(3)写出乙醛与新制氢氧化铜反应化学方程式;
(4)丙三醇与硝酸反应能生成三硝酸甘油酯,写出三硝酸甘油酯的结构简式
(5)下列有关实验的说法不正确的是_____________。
| A.制乙烯时,温度计应插入反应混合液中 |
| B.实验室用溴和苯在铁粉存在下反应,得到的溴苯显褐色,原因是溴苯在空气中被氧化 |
| C.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液 |
| D.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤 |
E.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热未产生砖红色沉淀,原因可能是NaOH量太少
桂醛在食品、医药、化工等方面都有应用。肉桂酸甲酯是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
(1)肉桂醛由C、H、O三种元素组成,质谱分析肉桂醛分子的相对分子质量为132,其分子中碳元素的质量分数为81.8%,肉桂醛的分子式是 。
肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原子,其结构简式是。(不考虑顺反异构与对映异构)
(2)已知:
I.醛与醛能发生反应,原理如下: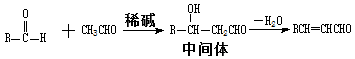
II.合成肉桂醛的工业流程如下图所示,其中甲为某种烃。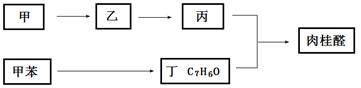
①甲的结构简式是。
②丙和丁生成肉桂的化学方程式是。
(3)肉桂醛能被银氨溶液氧化,再经酸化得到肉桂酸,写出肉桂酸甲酯的结构简式。
(4)现用芳香烃A为原料合成肉桂酸甲酯H的路线如下,测出A的核磁共振氢谱谱图有6个峰,其面积之比为1︰2︰2︰2︰1︰2。: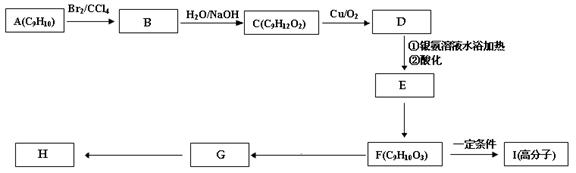
①化合物F中的官能团有 (填名称)。
②B→C的反应类型是 ,F→G的反应类型是 ,
③书写化学方程式
F→I
G→H
④G的同分异构体中,属于酯类目苯环上只有一个取代基的同分异构体有种。
其结构简式分别是
(1) 用系统命法写出下列物质名称或结构简式
2,2,3-三甲基丁烷的结构简式是
画出3-甲基-1-丁烯的键线式。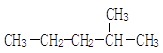 的系统命名是:
的系统命名是:
(2)写出下列反应的化学方程式
苯的硝化反应
乙烯发生加聚反应
乙醛与新制氢氧化铜反应
(1)下列各组化合物中,属于同系物的是(填入编号),属于同分异构体的是(填入编号)。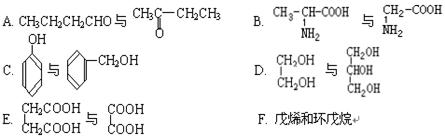
(2)有机物A: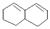 在加热条件下和Br2 按物质的量之比1:1发生的非邻位碳的加成反应
在加热条件下和Br2 按物质的量之比1:1发生的非邻位碳的加成反应
方程式
(3)某高分子有机物 是由一种单体缩聚而成的,该单体的结构简式为。
是由一种单体缩聚而成的,该单体的结构简式为。