磷单质及其化合物的、有广泛应用
(1)同磷灰石[主要成分]在高温下制备黄磷(P4)的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ;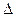 H
H
①上述反应中,副产物矿渣可用来 。
②已知相同条件下:
4Ca3(PO4)2F(s)+3SiO2(s)=6Cas3(PO4)2(s)+2CaSio3(s)+SiF4(g) ;△H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g);△H2
SiO2(s)+CaO(s)=CaSiO3(s) ;△H3
用△H1、△H2和△H3表示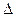 H,
H,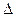 H= 。
H= 。
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式见下图)之间脱去两个水分子产物,其结构式为 。三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为 。

(3)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为 。
②化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a) Ni2+ + H2PO2-+ → Ni++ H2PO3-+
(b)6H2PO-2 +2H+ =2P+4H2PO3+3H2↑
请在答题卡上写出并配平反应式(a)。
③利用②中反应可在塑料镀件表面沉积镍—磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。
方法上的不同点: ;原理上的不同点: ;化学镀的优点: 。
(8)向20mL某物质的量浓度的AlCl3溶液中滴入2mol/L NaOH溶液时,得到的Al(OH)3沉淀的质量与所滴加的NaOH溶液的体积(mL)关系如下图所示,试回答下列问题: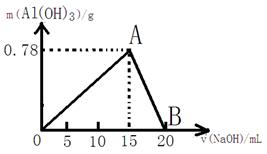
(1)上述两步反应用总的离子方程式可表示为:;
(2)若溶液中有Al(OH)3沉淀0.39g,则此时用去NaOH溶液的体积为。
(写出计算过程)
(7分)下图表示的反应关系中,部分产物被略去。已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A.无色液体B.无色气体C各1mol。X.E.G的焰色反应均为黄色。
回答下列问题: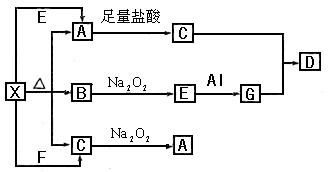
(1)写出下列物质的化学式:GD
(2)写出G与C反应生成D的化学反应方程式:
(3)写出X+E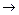 A的离子方程式:
A的离子方程式:
(4)写出C与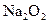 参加反应的化学方程式______________________________________,
参加反应的化学方程式______________________________________,
若0.2mol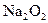 参加反应,则转移的电子数为_____________个。
参加反应,则转移的电子数为_____________个。
(5)写出物质X的用途(至少写出一种)______________________________________
某无色透明溶液,投入金属铝可放出H2。现有下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-。试判断下列两种情况时,各有哪些离子可存在于此溶液中:
(1)当生成Al3+时,可存在的离子有;
(2)当生成AlO2-时,可存在的离子有。
( 6分)除去下表各溶液中含有的少量杂质(括号内)填写下表:
| 物质(杂质) |
除杂质所需试剂 |
离子方程式 |
| Fe2O3(Al2O3) |
||
| FeCl2溶液(FeCl3) |
||
| NaHCO3溶液(Na2CO3) |
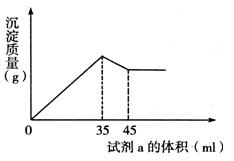
铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下: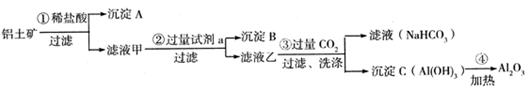
(1)沉淀 A、B的成分分别是、;
(2)步骤②中的试剂a是;
(3)试写出步骤③中发生反应的离子方式;
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如下图所示,则所用盐酸溶液的物质的量浓度为,样品中Al2O3的百分含量为。