在一定条件下,1mol N2和3mol H2混合后充分反应,达到平衡时测得平衡混合物的密度是同温同压下氢气的5倍,则氮气的转化率为 。若在同一个容器中,在相同的温度下,向容器中充入NH3,为使达到平衡时各成分的百分含量与上述平衡时相同,则起始时充入的NH3的物质的量为 。
(16分)物质的类别和核心元素的化合价是研究物质性质的两个基本视角。
(1)图中X的电子式为 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O(填“强”或“弱”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下,,得电子能力逐渐减弱。
(2)Na2S2O3是一种用途广泛的钠盐。
①下列物质用于Na2S2O3的从氧化还原反应的角度制备, ,理论上有可能的是(填字母序号)。
a.Na2S+S b.Z+S c.Na2SO3+Y d.NaHS+NaHSO3
②已知反应:Na2S2O3+H2SO 4Na2SO4+S↓+SO2↑+H2O。研究其反应速率时,下列说法正确的是(填写字母序号)。
4Na2SO4+S↓+SO2↑+H2O。研究其反应速率时,下列说法正确的是(填写字母序号)。
a.可通过测定一段时间内生成SO2的体积,得出该反应的速率
b.可通过比较出现浑浊的时间,研究浓度、温度等因素对该反应速率的影响
c.可通过Na2S2O3固体与稀硫酸和浓硫酸的反应,研究浓度对该反应速率的影响
(3)治理含CO、SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体。
①已知:CO(g)+1/2O2(g)=CO2(g) △H=-283kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-296kJ·mol-1
则治理烟道气反应的热化学方程式为。
②一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是(填写字母序号)。
a.v(CO)∶v(SO2)=2∶1
b.平衡常数不变
c.气体密度不变
d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为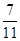 ,则SO2的转化率为。
,则SO2的转化率为。
(4)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式 。
(5)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表。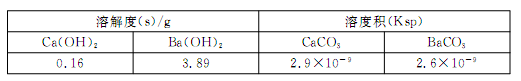
吸收CO2最合适的试剂是 (填“Ca(OH)2”或“Ba(OH)2”)溶液。
(12分)【选做题】本题包括A、B两小题,请选定其中一小题,并作答。若多做,则按A小题评分。
A.[物质结构与性质]原子序数小于36的X、Y、Z、W四种元素,X基态原子的最外层电子数是其内层电子数的2倍,Y基态原子的2p原子轨道上有3个未成对电子,Z是地壳中含量最多的元素,W的原子序数为22。
(1)W基态原子的核外电子排布式为________。元素X、Y、Z的电负性由大到小的顺序为________。
(2)与XYZ-互为等电子体的一种分子、一种离子分别为________、________(填化学式)。
(3)二元弱酸H2X2Z4中X原子轨道的杂化类型是_______,1 molH2X2Z4分子中含有σ键的数目为_______。
(4)YH3极易溶于水的主要原因是________________。元素W的氧化物WO2可与氢氟酸发生非氧化还原反应,生成配合物HnWF6,该反应的化学方程式为________。
(5)Z、W与Ca形成晶体的晶胞如图所示,该晶体的化学式为________。
(14分)CO和联氨(N2H4)的性质及应用的研究是能源开发、环境保护的重要课题。
(1)①用CO、O2和KOH溶液可以制成碱性燃料电池,则该电池反应的离子方程式为________。
②用CO、O2和固体电解质还可以制成如图1所示的燃料电池,则电极d的电极反应式为________。
(2)联氨的性质类似于氨气,将联氨通入CuO浊液中,有关物质的转化如图2所示。
①在图示的转化中,化合价不变的元素是________(填元素名称)。
②在转化过程中通入氧气发生反应后,溶液的pH将________(填“增大”、“减小”或“不变”)。转化中当有1 mol N2H4参与反应时,需要消耗O2的物质的量为________。
③加入NaClO时发生的反应为:Cu(NH3) +2ClO-+2OH-===Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
+2ClO-+2OH-===Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
该反应需在80℃以上进行,其目的除了加快反应速率外,还有________、________。
(3)CO与SO2在铝矾土作催化剂、773 K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应体系中各组分的物质的量与反应时间的关系如图3所示,写出该反应的化学方程式:________________。
【选做题】本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质]
高氯酸三碳酰肼合镍{[Ni(CHZ)3](ClO4)2 }是一种新型的起爆药。
(1)Ni2+基态核外电子排布式为。
(2)ClO4-的空间构型是;与ClO4-互为等电子体的一种分子为(填化学式)。
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为;1molCO(N2H3)2分子中含有σ键数目为。
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为a,Ni2+的配位数为b,NiO晶体中每个镍离子距离最近的镍离子数目为c,则a∶b∶c=。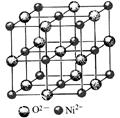
黄铁矿(主要成分FeS2)、黄铜矿(主要成分CuFeS2)均是自然界中的常见矿物资源。
(1)Stumm和Morgan提出黄铁矿在空气中氧化的四步反应如题20图-1所示:
① a反应中每生成1molFeSO4转移电子的物质的量为 mol。
② d反应的离子方程式为 。
(2)用细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高浸取速率,其原理如题20图-2
①冶炼过程中,正极周围溶液的pH (选填:“增大”、“减小”或“不变”)
②负极产生单质硫的电极反应式为 。
|
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见下表),其相关反应的平衡常数的对数值与温度的关系如题20图-3。
| 相关反应 |
反应热 |
平衡常数K |
FeS2(s) + H2(g)  FeS(s) + H2S(g) FeS(s) + H2S(g) |
ΔH1 |
K1 |
1/2 FeS2(s) + H2(g) 1/2Fe(s)+H2S(g) 1/2Fe(s)+H2S(g) |
ΔH2 |
K2 |
FeS(s) + H2(g) Fe(s)+H2S(g) Fe(s)+H2S(g) |
ΔH3 |
K3 |

①上述反应中,ΔH1 0(选填:“>”或“<”)。
②提高硫的脱除率可采取的措施有 (举1例)。
③1000K时,平衡常数的对数lgK1、lgK2和lgK3之间的关系为 。