我国规定饮用水质量标准必须符合下列要求:
| pH |
6.5~8.5 |
| Ca2+、Mg2+总浓度 |
<0.0045mol·L-1 |
| 细菌总数 |
<100个/mL |
某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意
图如下: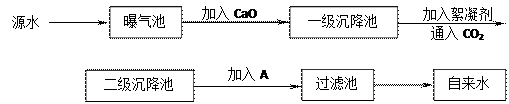
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入CaO后生成,进而发生若干个化学反应,请写出其中任意一个反应的离子方程式 。
(2)加入絮凝剂可以除去其中的悬浮固体颗粒,该过程是 (填写序号)。
①只有物理过程,无化学过程
②只有化学过程,无物理过程
③既有物理过程,又有化学过程
(3)FeSO4·7H2O是常用的絮凝剂,加入后最终生成红褐色胶状沉淀,则这种沉淀是 (填写化学式)。
(4)通入二氧化碳的目的是 和 。
(5)物质A的作用是 ,则A可以选择下列物质中的 (填写序号)。
①ClO2 ②SO2 ③液氯 ④Ca(ClO2)2 ⑤浓硫酸
(12分)合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响。合成氨反应的化学方程式为:N2(g)+3H2(g) 3NH3(g) ,△H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。回答下列问题:
3NH3(g) ,△H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。回答下列问题:
(1) 合成氨工业中原料气压缩到30~50MPa的原因是 。从平衡移动原理分析,低温有利于原料气的转化,实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,原因之二是。
。从平衡移动原理分析,低温有利于原料气的转化,实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,原因之二是。
(2) 500℃、50MPa时,在容积为VL的容器中加入nmolN2、3nmolH2,反应达平衡后测得平衡常数为K1,此时N2的转化率为x。则K1和x的关系满足K1=。若温度为400℃,平衡常数为K2,则K1K2(填“<”、“=”或“>” )
(3) 甲烷在高温下与水蒸气反应的热化学反应方程式为:
CH4(g)+H2O(g)=CO(g)+3H2(g); △H kJ·mol-1。
又已知: H2(g) +1/2 O2(g)="=" H2O(l);△H1=-285.8kJ/mol
CO(g) + 1/2 O2(g)=CO2(g) ;△H2=-283.0kJ/mol
CH4(g) +2 O2(g)="=" CO2(g) + 2H2O(l); △H3=-890.3kJ/mol
H2O(g) ="=" H2O(l); △H4=-44.0kJ/mol
①写出H2(g)完全燃烧生成气态水的热化学方程式。
② CH4(g)+H2O(g)=CO(g)+3H2(g); △H=kJ/mol
淡黄色固体A和气体X存在如下转化关系:
请回答下列问题
(1)固体A的名称,X的化学式。
(2)反应③的化学方程式为。
(3)写出反应②④的离子方程式:
反应②。
反应④。
(4)溶液 C中的阴离子主要是_
C中的阴离子主要是_ _________,检验该离子的实验操作为______________
_________,检验该离子的实验操作为______________
_________________________________。
化学计量在化学中占有重要地位,请回答下列问题:
(1)现有mg某气体,它由双原子分子构成,其摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为___ _____;
_____;
②该气体所含原子总数为个;
③该气体在标准状况下的体积为__________。
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是_______(用分式表示)。
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是______________。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO42 -,测得Na+、Mg2
-,测得Na+、Mg2 +和Cl-
+和Cl-
的物质的量浓度依次为:0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c(SO42-)="___________" 。
现有以下5种物质:H2O、SiO2、CaO、Na2O2、Al2O3。
(1)按照不同的分类标准,它们中有一种物质与其它物质有明显的不同,请找出这种物质并写出依据(试写出任意一种合理的分类方法):
。
(2)上述物质中有些可以两两反应,试写出一个属于氧化还原反应的离子反应方程式__________ ______________________________________________________________。
______________________________________________________________。
图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下气态化合物,C为常温下液态化合物,图中有部分生成物未标出。请填写以下空白: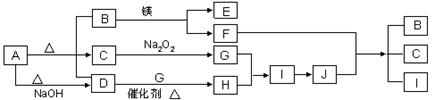
(1)写出下列反应的化学方程式:
D+G→ H,
F+J → B + C + I。
(2)写出A+NaOH→D的离子方程式。
(3)J的浓溶液久置后显黄色,其原因用化学方程式表示为_________________________。