下列说法不正确的是
A.配制FeCl2溶液时,可将FeCl2晶体先溶于浓盐酸,再加水稀释和少量铁屑保存
B.输油管道,为防止其表面被腐蚀应涂上隔水材料并与外电源负极相连
C.pH值均为9的NaOH溶液和Na2CO3溶液,两溶液中水的电离程度相同
D.0.1mol/L 弱酸HA溶液与0.05mol/L NaOH溶液等体积混合后所得溶液微粒浓度间有: 2c(H+)+c(HA) = c(A-)+2 c(OH-)
下列实验中,依据实验操作及现象,得出的结论正确的是
| 操 作 |
现 象 |
结 论 |
|
| A |
测定等浓度的Na2CO3和Na2SO4 溶液的pH |
前者pH比后者的大 |
非金属性: |
| B |
将一片铝箔置于酒精灯外焰上灼烧 |
铝箔熔化但不滴落 |
铝箔表面有致密Al2O3薄膜,且Al2O3熔点低于Al |
| C |
向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 |
生成白色沉淀 |
溶液X中一定含有 或 或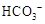 |
| D |
取久置的Na2O2粉末,向其中滴加过量的盐酸 |
产生无色气体 |
Na2O2没有变质 |
下列反应的离子方程式正确的是
| A.次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+ H2O +CO2=CaCO3↓+2HClO |
| B.硫酸亚铁溶液中加过氧化氢溶液 Fe2++2H2O2+4H+=Fe3++4H2O |
| C.Fe2(SO4)3的酸性溶液中通入足量硫化氢 Fe3++H2S=Fe2++S↓+2 H+ |
| D.氯化亚铁溶液中加入稀硝酸 3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B.通入过量SO2气体后的溶液:H+、Ca2+、Fe3+、NO3- |
| C.通入足量CO2的溶液:H+、NH4+、Al3+、SO42- |
| D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
已知NA代表阿伏加德罗常数,下列说法正确的是
| A.在1 L 0.1 mol·L-1氟化钠溶液中含有F-和HF数目之和为0.1NA |
| B.300 mL 2 mol/L蔗糖溶液中所含分子数为0.6NA |
| C.标准状况下,1.8gD2O中含有NA个中子 |
| D.标准状况下,2.24 L三氯甲烷中含有氯原子数目为0.3NA |
化学知识在生产和生活中有着重要的应用.下列说法中正确的是
①铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
②发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
③纯净的二氧化硅是现代光学及光纤制品的基本原料
④Na2O2既可作呼吸面具中O2的,又可漂白织物、麦杆、羽毛等
⑤碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑥明矾常作为消毒剂
| A.①②③④ | B.①②③⑤ | C.①②④⑥ | D.①②③④⑤⑥ |