实验室用右图所示的装置制取溴乙烷。在试管I中依次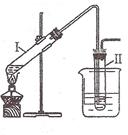
加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠
粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管
I至微沸状态数分钟后,冷却。
试回答下列问题:
(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式 _______ 。
(2)试管I中反应除了生成溴乙烷,还可能生成的有机物有 _______ (任写两种结构简式)。
(3)设计实验证明试管Ⅱ收集的溴乙烷中含有溴元素,完成以下实验报告:
| 实验步骤 |
实验操作 |
预期现象和结论 |
| 1 |
_______ |
_______ |
| 2 |
_______ |
_______ |
| 3 |
_______ |
_______ |
| 4 |
_______ |
_______ |
(4)设计实验方案,检验溴乙烷与NaOH乙醇溶液发生消去反应后生成的气体X中是否含乙烯。在答题卡对应的方框中画出实验装置图,并注明所用试剂的名称。
写出下列反应的热化学方程式:(6分)
(1) 32.5g锌在氧气中完全燃烧生成氧化锌固体,放出175KJ的热量。
。
(2) 氢气与碘蒸气反应,生成1molHI气体时,吸收25.9KJ的热量;
。
甲、乙两个容器中,分别加入0.1mol/L NaCl溶液与0.1mol/L AgNO3溶液后,以Pt为电极进行电解时, (14分)
(14分)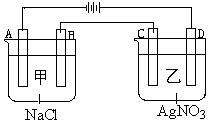
(1)写出电极名称和电极反应式:
A
B
C
D
(2)在A、D电极上生成的气体物质的量之比为:_____________
已知在29 8K时的热化学反应方程式:(3分)
8K时的热化学反应方程式:(3分)
C(s,石墨)+O2(g)=CO2(g);△H1=-393.5kJ/mol,
2CO(g)+O2(g)=2CO2(g);△H2=-566.0kJ/mol。
则298K时,反应 C(s,石墨)+1/2 O2(g) =" CO" (g)的△H是______________
黑火药的成分是硝酸钾、硫磺、木炭。当加热或点燃时会发生剧烈反应而爆炸。生成物中硫元素变为最低价,碳、氮两元素均变成空气中常见的气体。
(1)写出有 关反应的化学方程式:___________________________________________
关反应的化学方程式:___________________________________________
(2)10.1g KNO3完全反应时,被它氧化的碳为_______g。
A、B、C、D、E、F 六种物质有如下变化关系,E是淡黄色粉末,判断: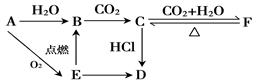
(1)写出下列物质的化学式:
A._____ _____; D.____________ ;
(2)写出有关反应的化学方程式(是离子反应的直接写离子方程式)
B―→C:_____________________________________
E―→B:________________________________________
C―→F:_________________________________________
F―→C:_____________________________________