我们用字母L、M、Q、R、X分别代表五种含不同化合价的氮元素的物质,并且每种物质中氮元素的化合价只有一种。又知道物质L中氮元素的化合价要比物质M中氮元素的化合价低,并且在一定条件下,它们会有如下的相互转换关系(未配平):
①Q+HCl→M+Cl2;
②R+L→X+H2O;
③R+O2→L+H2O.
(1)已知这五种物质中有一种是硝酸,那么硝酸应该是L、M、Q、R、X中的________(填字母),判断的依据是_________________________________________________。
(2)反应③是在催化剂(如铂、氧化铁等)存在,并且加热到一定温度时发生的,这个反应在工业上有重要的应用。请据此推断,若物质X是密度比CO2密度小的气体,那么X的化学式是__________.
(3)某同学写出下面三个不同价态的氮的化合物相互转换的关系(未配平):
a、NO+HNO3→N2O3+H2O
b、NH3+NO→HNO2+H2O
c、N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是________________________________(填编号).
(选考题)锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)锰元素位于第四周期第ⅦB族。基态Mn2+的核外电子排布式为。NO3-的空间构型为________。
(2)HCHO中含有的σ键和π键数目之比为________。
(3)火山喷出的岩浆中含有多种硫化物,冷却时ZnS比HgS先析出,原因是
(4)Cu3N形成的晶体结构如图所示。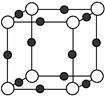
则与同一个N3-相连的Cu+有________个,Cu+的半径为a pm,N3-的半径为b pm,
则Cu3N的密度为g·cm-3。(只列式,不用计算出结果)(阿伏加德罗常数用NA表示,1 pm=10-10 cm)
(共15分)甲醇合成反应及其能量变化如图所示: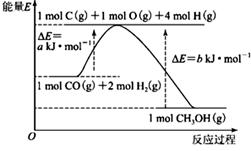
(1)写出合成甲醇的热化学方程式 。
(2)实验室在1 L的密闭容器中进行模拟合成实验。将1 mol CO和2 mol H2通入容器中,分别恒温在300 ℃和500 ℃反应,每隔一段时间测得容器内CH3OH的浓度如下表所示:
| 时间浓度(mol/L)温度 |
10 min |
20 min |
30 min |
40 min |
50 min |
60 min |
| 300 ℃ |
0.40 |
0.60 |
0.75 |
0.84 |
0.90 |
0.90 |
| 500 ℃ |
0.60 |
0.75 |
0.78 |
0.80 |
0.80 |
0.80 |
(2)在300 ℃反应开始10 min内,H2的平均反应速率为v(H2)。
(3)在500 ℃达到平衡时,平衡常数K=________。
(4)在另一体积不变的密闭容器中,充入1.2 mol CO和2.0 mol H2,一定条件下达到平衡,测得容器中压强为起始压强的一半。计算该条件下H2的转化率为________。
(5)铜基催化剂具有活性高、选择性好和条件温和的特点,已广泛地使用于CO/CO2的加氢合成甲醇。使用铜基催化剂后,该反应中a的大小变化对反应热ΔH有无影响?(填有或无)_____________。
(6)2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如图所示。
请写出从C口通入O2发生的电极反应式。
(7)用上述电池做电源,用下图装置电解饱和食盐水(C1、C2均为石墨电极)。
①该反应的离子方程。
②电解开始后在电极___________的周围(填“C1”或“C2”)先出现红色。
A、B、D、E、W是元素周期表前四周期中常见的元素,其相关信息如下表:
| 元素 |
相关信息 |
| A |
A原子L层电子数是K层电子数的2倍 |
| B |
B是地壳中含量最多的元素 |
| D |
在第3周期元素中,它的简单离子半径最小 |
| E |
E存在质量数为23,中子数为12的核素 |
| W |
W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)W位于元素周期表的位置是。
(2)A 和B的气态氢化物中,较稳定的是_________(写化学式);E2B2的电子式表示为。
(3)写出W的白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色这个过程的化学方程式:。
(4)写出D和B组成的二元化合物与E的最高价氧化物的水化物反应的离子方程式:
。
(5)将一定质量的Mg和D的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则固体混合物中D的质量为;原稀硫酸溶液的物质的量浓度为。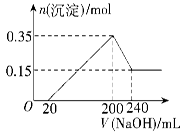
 新型锂离子电池在新能源的开发中占有重要地位。可用作节能环保电动汽车的动力电池。磷酸亚铁锂(LiFePO4)是新型锂离子电池的首选电极材料,它的制备方法如下:
新型锂离子电池在新能源的开发中占有重要地位。可用作节能环保电动汽车的动力电池。磷酸亚铁锂(LiFePO4)是新型锂离子电池的首选电极材料,它的制备方法如下: 方法一:将碳酸锂、乙酸亚铁[(CH3COO)
方法一:将碳酸锂、乙酸亚铁[(CH3COO)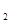 Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。
Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。 方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。
方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。 在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:
在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:
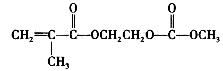
 请回答下列问题:
请回答下列问题: (1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是
(1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是 。
。 (2)在方法一所发生的反应中, 除生成磷酸亚铁锂、乙酸外,还有、
(2)在方法一所发生的反应中, 除生成磷酸亚铁锂、乙酸外,还有、 、(填化学式)生成。
、(填化学式)生成。 (3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为
(3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为 。
。 (4)写出M与足量氢氧化钠溶液反应的化学方程式:
(4)写出M与足量氢氧化钠溶液反应的化学方程式: 。
。 (5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为
(5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为 。
。
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
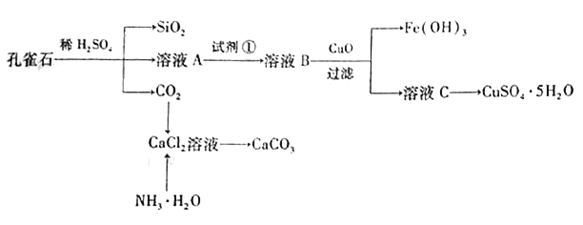
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为______(填代号),检验溶液A中Fe3+的最佳试剂为(填代号)。
a.KMnO4b.(NH4) 2S c.H2O2d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是。
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)(填化学式),若实验过程中有氨气逸出,应选用下列装置回收(填代号)。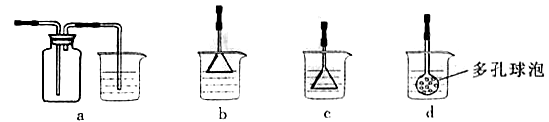
 (4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应,直到,用KMnO4标准溶液滴定时应选用滴定管(填“酸式”或“碱式”)。
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应,直到,用KMnO4标准溶液滴定时应选用滴定管(填“酸式”或“碱式”)。