空气质量越来越爱到人们的关注,下表是部分城市某日的空气质量报告:
| 城市 |
污染指数 |
首要污染物 |
空气质量级别 |
空气质量状况 |
| 北京 |
89 |
NOx |
Ⅱ |
良 |
| 上海 |
49 |
— |
Ⅰ |
优 |
| 宁波 |
55 |
SO2 |
Ⅱ |
良 |
| 克拉玛依 |
106 |
PM10 |
Ⅲ1 |
轻微污染 |
(1)由上表可知,在上述城市中,容易出现酸雨的城市有: ;空气质量最差的成都市是: 。
(2)可吸入颗粒(PM10)又称为飘尘,它与空气中的SO2、O2接触时,使部分的SO2转化为SO3,使空气酸度增加,形成酸雨。飘尘所起的主要作用是( )。
A.氧化剂 B.还原剂 C.吸附剂 D.催化剂
(3) 汽车排放的尾气、硝酸和化肥厂等工厂排出的废气中都含有氮氧化物,氮氧化物溶于水最终转化为 ,这也是造成酸雨的另一个主要原因。
(4) 酸雨可导致下列哪种危害( )
A.腐蚀建筑物 B.导致树木枯萎 C.造成洪涝灾害 D.影响湖泊生态环境
(5) 根据上表,请你提出改善北京空气质量的一项建议。
(17分)I.工业上有一种用CO2来生产甲醇燃料的方法:
将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。图中数据a(1,6)表示:在1 min时H2的物质的量是6 mol。
(1)a点正反应速率(填“大于”“等于”或“小于”)逆反应速率。其化学平衡常数K=
(2)下列时间段平均反应速率最大的是,
| A.O~1 min | B.1~3 min | C.3~8 min | D.8~11 min |
(3)仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示。曲线I对应的实验条件改变是,曲线Ⅱ对应的实验条件改变是,体积不变再充入3molCO2和4 mol H2,H2O(g)的体积分数(填“增大”“不变”或“减小”)
Ⅱ.某实验小组欲探究反应速率与温度的关系,现有1mol/L的KI溶液、0.1mol/L的H2S04溶液、淀粉溶液,则实验时这几种试剂的加入顺序为:KI溶液、、;
反应的方程式为
Ⅲ. 粗镍样品中含Fe、Zn、Ag、Cu等四种金属杂质,为获得高纯度的镍,某兴趣小组同学拟用铅蓄电池为电源,粗镍及石墨为电极,电解硝酸镍溶液对粗镍进行提纯。
(1)电解结束后,在阳极附近的沉淀物中,主要的金属单质为(填化学式)。
(2) 若按上图所示连接对铅蓄电池进行充电。充电一段时间后。则在A电极上生成(填化学式)。B电极上的电极反应式为;充电完毕。铅蓄电池的正极是极(填“A”或“B”)。
(3)如用甲烷燃料电池为电源,在25℃、101 kPa时,若CH4在氧气中直接燃烧生成1 mol水蒸气放热401 kJ,而l g水蒸气转化成液态水放热2.445 kJ,则CH4的燃烧热为(取整数)kJ·mol-。
A、B、C、D、E、F六种化合物。其中A、B、C、D、E均由短周期元素组成,焰色反应均呈黄色,B、C、E均由三种元素组成,B、C的组成元素相同,且C的摩尔质量比B大80g/mol请回答下列问题:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为(填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)下表为B与F实验的部分内容:
| 序号 |
主要实验步骤及实验现象 |
| ① |
在含有B的溶液中,加入稀H2S04,产生浅黄色浑浊和无色有刺激性气味的气体。 |
| ② |
20 ml沸水中滴加F的饱和溶液1~2ml,所得液体呈红褐色 |
| ③ |
将实验②得到的红褐色液体加热蒸发、灼烧,最终得到红棕色固体 |
写出B与稀H2S04反应的离子方程式:;
写出②中反应的化学方程式:。
(3)现由6种粒子Mn2+、MnO4一、H十、H2 0、X2Y82一(C中含有的阴离子)、XY42一完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4一需氧化剂的物质的量为。
(4)化合物D和E可以相互转化: 若有D和E·XH20的混合物13.04g,加热到完全反应后,气体产物通过浓H2S04增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为,E·XH20的化学式为。
若有D和E·XH20的混合物13.04g,加热到完全反应后,气体产物通过浓H2S04增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为,E·XH20的化学式为。
(14分)某学生实验小组拟用孔雀石(主要成分是Cu(OH)2·CuC03,其杂质主要为FeC03等)制胆矾,实验设计流程如下:
回答下列问题:
(1)步骤(a)中,实验研磨孔雀石的仪器名称;用硫酸浸取的化学方程式:
(2)步骤(b)中,pH控制在3.O~3.5,其目的是;加过氧化氢发生反应的离子方程式为。
(3)怎样判断蒸发浓缩已完成:。
(4)将制得的样品用热重仪进行热重分析,热重仪原理及热重记录如下表:
写出212~248℃温度范围内发生反应的化学方程式。
(5) FeC03为白色沉淀,此沉淀的Ksp(FeC03)=2×10-11,将FeCl2的稀溶液与Na2CO3溶液等体积混合,若FeCl2的浓度为2×lO一5mol·L-1.则生成沉淀所需Na2CO3溶液的最小浓度为mol·L-1。
为了检验淀粉水解的产物,某学生设计了如下实验方案:
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是:作用。
(2)试剂2为 溶液,其作用是;
发生反应的离子方程式为:。
(3)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是。
苯是最重要的基本有机化工原料之一,现利用苯,同时使用其他部分试剂,可实现如下转化: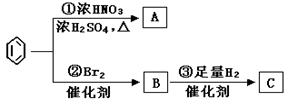
请回答下列问题:
(1)写出下列反应的化学方程式:
反应①:;反应②:;
(2)上述反应①~③中,属于加成反应的是 (填序号)。
(3)C的结构简式为:。