将一小块钠投入CuSO4溶液中,请写出有关反应的化学方程式:
、 。
(1)配平氧化还原反应方程式:
▲ C2O42- +▲ MnO4- +▲ H+=▲ CO2 +▲ Mn2++▲ H2O
(2)称取5.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶液。量取两份此溶液各25mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至16mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为▲ mol;
②第二份溶液中滴加0.10mol·L-1的酸性高锰酸钾溶液至12 mL时反应完全,则该溶液中还原剂的物质的量为▲ mol;
③原试样中H2C2O4·2H2O的质量分数是▲和KHC2O4的质量分数是▲。
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166 g·mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术。ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+。
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是▲> ▲> ▲。
(2)铁酸钠之所以能净水,除它本身具有强氧化性外,另一个原因可能是▲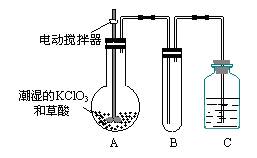
(3)二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐。工业上用稍潮湿的KClO3和草酸在60℃时反应制得。某学生用如上图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。请问:
①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置▲;
②该装置按①补充完整后,装置A、B、C中还有一处设计明显不合理的是▲ _(填“A、B或C”),理由是▲
③C中应装的试剂为 ▲。
C中发生反应的离子方程式为:▲。
某研究性学习小组用10g胆矾制取CuO,并证明CuO可以催化H2O2的分解反应。
(1)首先制备CuO,实验步骤如下,请完成缺少的步骤:
①称取10g胆矾,放入小烧杯中,再加水溶解;
②向小烧杯中滴加NaOH溶液,至产生大量沉淀;
③用酒精灯在石棉网上加热小烧杯,至沉淀物完全黑色;
④将以上混合物过滤,洗涤,▲,然后研细;
⑤检查④中洗涤是否完全的操作是▲。
(2)用右图所示,按表中设计实验方法,证明CuO能催化
7%H2O2 溶液的分解,并与MnO2的催化效果进行比较。
| 实验序号 |
双氧水体积 |
催化剂 |
待测数据 |
| a |
15mL |
无 |
|
| b |
15mL |
0.5g CuO |
|
| c |
15mL |
0.5g MnO2 |
① 从设计原理看,实验中的待测数据是▲。
② 为探究CuO在实验b中是否起催化作用,除与a比较外,还应补充以下实验(不必写具体操作):
A.证明CuO▲性质(选填“物理性质”或“化学性质”)在反应前后是否改变;
B.▲。
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去)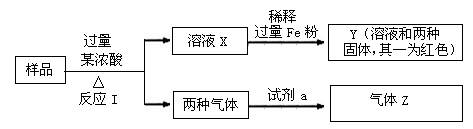
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)▲ 。
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应I中能同时生成两种气体的化学方程式是▲ 。
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是▲ 。
(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)
▲ 。
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是▲ 。
(5)另取原样品,加入足量稀硫酸充分反应。若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中的物质用化学式表示)▲ 。
有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、I-、NO3-、CO32-、SO42-中的几种。取该溶液进行以下实验:
①用pH试纸检验,表明溶液呈强酸性。
②取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色。
③另取部分溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,均无沉淀产生。
④另取部分上述碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
⑤将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定:
(1)写出⑤所发生反应的离子方程式▲
(2)该溶液中肯定存在的阳离子是▲
(3)该溶液中肯定不存在的阴离子是▲