某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)混合气体中气态烷烃的化学式: 。
(2)混合气体中两种气体的物质的量之比: 。
(3)写出混合气体中气态烯烃可能的结构简式: 。
金属镁可用于制造合金、储氢材料、镁电池等。
已知:①C(s)+O2(g) CO(g) ΔH="-110.5" kJ·mol-1②Mg(g)+O2(g)
CO(g) ΔH="-110.5" kJ·mol-1②Mg(g)+O2(g) MgO(s) ΔH="-732.7" kJ·mol-1
MgO(s) ΔH="-732.7" kJ·mol-1
(1)一种制备镁的反应为MgO(s)+C(s) Mg(g)+CO(g),该反应的ΔH=。
Mg(g)+CO(g),该反应的ΔH=。
(2)一种用水氯镁石(主要成分为MgCl2·6H2O)制金属镁工艺的关键流程如下:
①为探究MgCl2·6H2O“一段脱水”的合理温度范围,某科研小组将MgCl2·6H2O在不同温度下分解,测得残留固体物质的X-射线衍射谱图如下图所示(X-射线衍射可用于判断某晶态物质是否存在)。测得E中Mg元素质量分数为60.0%,则E的化学式为。 “一段脱水”的目的是制备MgCl2·2H2O,温度不高于180 ℃的原因是。
②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率。生成MgO的化学方程式为 。 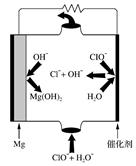
(3)Mg2Ni是一种储氢材料。2.14 g Mg2Ni在一定条件下能吸收0.896 L H2(标准状况下)生成X,X的化学式为。
(4)“镁-次氯酸盐”燃料电池的装置如右图所示,该电池反应的电极反应式分别为负极。 正极
水滑石(MgaAlb(OH)c(CO3)d·xH2O)用作阻燃剂及催化剂的载体
(1)MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为。
(2)为确定水滑石的组成,进行如下实验:取水滑石样品60.2g进行加热时,温度与剩余固体质量的关系如图。认真分析图中曲线变化情况回答下列问题(已知样品在400℃时已完全失水)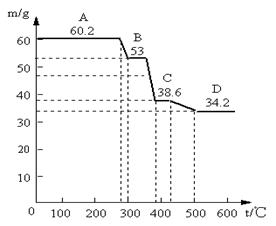
①当温度在0~280℃质量不变,是什么原因:。C→D减少的物质其物质的量为
②该水滑石的化学式为(写出计算过程)
某铝土矿中主要含有Al2O3、Al(OH)3、AlO(OH),还含有Fe2O3等杂质。利用拜耳法生产氧化铝的流程如下图所示: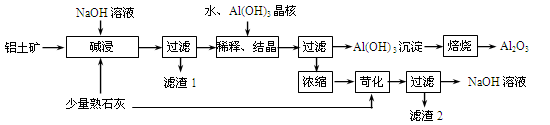
(1)碱浸时为提高铝土矿的浸出率可采取的措施是,。(答两点)
(2)AlO(OH)与NaOH反应的化学方程式为。
(3)在稀释、结晶过程中,加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工艺,也可用通入足量的某气体的方法来代替。通入气体时发生反应的离子方程式是.
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式:。
(5)该生产流程能实现(填化学式)的循环利用。
(6)氧化铝是工业上冶炼铝的原料,用氧化铝电解制备金属铝时需加入冰晶石(Na3AlF6)作助熔剂,写出用NaF和Al2(SO4)3反应制备冰晶石的化学方程式为 。
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题。
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1。
则CH4与O2反应生成CO和H2的热化学方程式为______________________________。
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为2L 2mol/LKOH溶液),通过装置Ⅱ制备稀H2SO4。若持续通入甲烷,在标准状况下,消耗甲烷的体积V L。
①0<V≤44.8时,装置Ⅰ的总反应方程式为:。
②44.8<V≤89.6时,装置Ⅰ中负极电极反应为:。
③装置Ⅱ中C棒上的电极反应式为:。
④ 若装置Ⅰ中消耗的甲烷在标况下的体积为22.4L,则装置Ⅱ中理论上生成的H2SO4的物质的量为mol。
计算多元弱酸(HnX)溶液的c(H+)及比较弱酸的相对强弱时,通常只考虑第一步电离。回答下列关于多元弱酸HnX的问题。
(1)若要使HnX溶液中c(H+)/c(HnX)增大,可以采取的措施是。
A.升高温度B.加少量固态HnXC.加少量NaOH溶液D.加水
(2)用离子方程式解释NanX呈碱性的原因:。
(3)若HnX为H2C2O4,且某温度下,H2C2O4的K1=5×10-2、K2=5×10-5.则该温度下,0.2mol/L H2C2O4溶液 中c(H+)约为mol/L。(已知
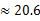 )
)
(4)已知KHC2O4溶液呈酸性。
①KHC2O4溶液中,各离子浓度由大到小的顺序是 。
②在KHC2O4溶液中,各粒子浓度关系正确的是。
A.c(C2O42-)<c(H2C2O4)
B.c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
C.c(K+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-)
D.c(K+)= c(C2O42-)+ c(HC2O4-)+ c(H2C2O4)