有下列实验装置如图:
示意图中A是简易的氢气发生器,B是大小适宜的圆底烧瓶,C是装有干燥剂的U形管,a是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞的试管。
实验前先检查实验装置的气密性。实验开始时,先关闭活塞a,并取下烧瓶B;向A中加入一定量适当浓度的盐酸,产生氢气。经必要的“操作”〔见问题(2)〕后,在导管的出口处点燃氢气,然后如图所示套上烧瓶B,塞紧瓶塞,氢气在烧瓶中继续燃烧,用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞a,气体通过反应管D进入试管E中,使酚酞试液呈红色。请回答下列问题。
(1)实验前如何检查装置的气密性:</PGN0035B.TXT/PGN>____。
(2)点燃氢气前必须进行____操作,进行该操作的方法是____。
(3)写出B、D中分别发生反应的化学方程式:
B中_______________
D中________________
(4)C中所盛干燥剂的名称是____;该干燥剂的作用是____。
用如图所示的装置进行制取NO实验(已知Cu与HNO3的反应是放热反应)。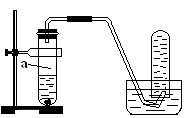
(1)在检查装置的气密性后,向试管a中加入10ml 6 mol·l-1稀HNO3和1gCu片,然后立即用带导管的橡皮塞塞紧试管口。请写出Cu与稀HNO3反应的化学方程式:_______________________________________________________。
(2)实验过程中通常在开始反应时反应速率缓慢,随后逐渐加快,这是由于
_________________________________________________; 进行一段时间后速率
又逐渐减慢,原因是______________________________________________。
(3)欲较快地制得NO,可采取的措施是_____________。
| A.加热 | B.使用铜粉 | C.稀释HNO3 | D.改用浓HNO3 |
(14分)某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此实验小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。已知:常温下,CO能使一些化合物中的金属离子还原。
例如:PdCl2+CO+H2O=Pd↓+CO2+2HCl
反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。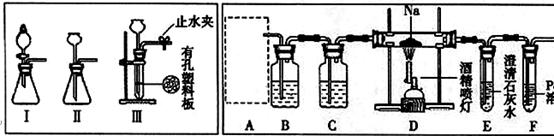
请回答下列问题:
(1)为了使制气装置能“随开随用,随关随停”,上图A处制取CO2气体应选用的装置
是 (填写“I”、“II”或“III”),其离子方程式是 ,。装置B、C中应盛放的试剂分别是 。
(2)观察实验装置图可知Na与CO2反应的条件是 ,检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是 ,待装置E 中出现 现象时,再点燃酒精喷灯。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是 。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是 。
|
(4)请判断②中D装置生成固体的成分是钠的正盐还是酸式盐?请用文字简要说明理由。
(12分)非金属单质A经如下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题: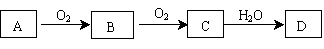
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
① D的化学式是 。
②在工业生产中B气体的大量排放被雨水吸收后形成了 而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体
①A、C的化学式分别是:A C 。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式 。
该反应 (填“属于”、“不属于”)氧化还原反应。
(13分)某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式:2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2H2O
CaCl2 + 2NH3↑+ 2H2O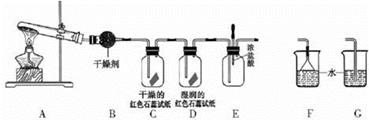
【实验探究】
(1)A中的反应 (填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取气体 (只填一种)
(3)若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是 L(NH4C1的摩尔质量为 53.5g·mol-1)。
(4)实验室收集氨气的方法是
(5)C、D装置中颜色会发生变化的是 (填“C”或“D”)
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,可观察到的现象是 。
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是 (填“F”或“G”)。
【知识拓展】
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O==Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列 物质代替(填序号)。
A.碱石灰(NaOH与CaO的固体混合物) B.NaOH固体
C.硫酸溶液 D.石灰石(含CaCO3)
【知识应用】
(9)2010年11月9日晚,我省宁德市一冷冻厂发生氨气泄漏事件,500多居民深夜大转移。假如你在现场,你会采用什么自救为法? 。
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O)。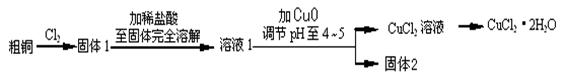
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。
① 仪器A的名称是 。
② 装置B中发生反应的离子方程式是 。
③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”) 。
④装置Ⅳ中盛装的试剂是,其作用是。
(2)在CuCl2溶液转化为CuCl2·2H2O的操作过程中,发现溶液颜色由蓝色变为黄绿色。小组同学欲探究其原因。
已知:在氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq) +4Cl-(aq)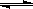 CuCl42-(aq) +4H2O(l)
CuCl42-(aq) +4H2O(l)
蓝色 黄色
①上述反应的化学平衡常数表达式是K= 。
若增大氯离子浓度,K值(填“增大”、“减小”或“不变”) 。
②现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法
a.b.。