某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)====CuSO4+H2↑。
(1)请在方框内画出能够实现这一反应的实验装置图。
| |
(2)某同学在做铜与稀硫酸的上述反应实验时,看到碳棒和铜棒都有气泡产生,但铜棒没有被腐蚀。请你分析其原因___________________,此时的电池反应为____________________。
( 12分)某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
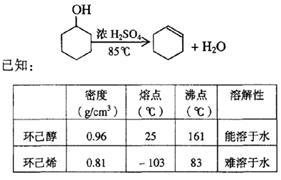

 .
.
|
|||
|
|||
|
化学是一门以实验为基础的自然科学,

化学实验在化学学习中具有重要的作用。
(1)右图分别是温度计、量筒、滴定管的一部分,
其中A仪器的名称为,
B的正确读数为。
(2)实验室很难配制准确浓度的NaOH溶液,需要 用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。
用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。
①该学生用托盘天平称量时,先在两边托盘上放等质量的纸片,取少量邻苯二甲酸氢钾置于左盘,只用游码(单位:g)调整平衡时如下图所示。由此可知,所取邻苯二甲酸氢钾的质量为g。
②将称好的邻苯二甲酸氢钾置于锥形瓶中,加适量蒸馏水完全溶解得到无色溶液,再加入1~2滴指示剂,当观察到现象时,可停止滴定,记录数据。
③该学生进行了三次实验,所取固体质量均相同,达到滴定终点时记录所用未知氢氧化钠溶液的体积如下表:
| 实验编号 |
NaOH溶液的体积(mL) |
| 1 |
22.52 |
| 2 |
22.49 |
| 3 |
22.50 |
则计算氢氧化钠溶液物质的量浓度的表达式为:(用数据表示,不需计算)
④以下操作会造成NaOH溶液浓度偏高的是(填序号)
| A.未用氢氧化钠溶液洗涤碱式滴定管 |
| B.滴定前平视,滴定后俯视读数 |
| C.滴定前滴定管尖嘴有气泡,滴定后气泡消失 |
| D.滴定前未用邻苯二甲酸氢钾溶液洗锥形瓶 |
测定水中溶液氧气的方法是:取a mL水样,迅速加入MnSO4溶液及含有NaOH的KI溶液,立即塞上塞子、振荡,使之充分反应;打开塞子,迅速加入适量的稀硫酸,此时有I2生成;再用Na2S2O3溶液(浓度b mol/L)和I2反应,消耗了VmL达到终点(以淀粉作指示剂)。有关方程式为:①2Mn2++O2+4OH-=2MnO(OH)2(反应很快);②MnO(OH)2+2I-+4H+=Mn2++I2+3H2O;③I2+2S2O32-=S4O62-+2I-。
⑴需要进行滴定的反应是,终点的颜色变化为。
⑵将Na2S2O3溶液盛放在(“酸式”或“碱式”)滴定管中。
⑶在加入MnSO4溶液及含有NaOH的KI溶液和适量的稀硫酸时,要迅速的加入,否则将对结果造成(“偏高”、“偏低”或“无影响”),原因是
。
⑷在加入MnSO4溶液及含有NaOH的KI溶液振荡时,塞子未塞紧,溅出部分溶液,则将对结果造成(“偏高”、“偏低”或“无影响”),原因是
。
⑸水中溶液O2为(以m g/L为单位)。
从环己烷可制备1,4-环己二醇的二醋酸酯,下列有关的8步反应(其中所有无机产物都已略去):
其中有3步属于取代反应,2步属于消去反应,3步属于加成反应。
反应①____和____属于取代反应。
化合物的结构简式是:B____,C_____。
反应④所用试剂和条件是_______。
向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再生成二氧化碳气体为止,则在此过程中,溶液中的碳酸氢根离子浓度变化趋势可能是:
| A.逐渐减小; | B.逐渐增大; | C.先逐渐增大,而后减小; | D.先逐渐减小,而后增大。你的选择是____(填正确选项的标号)。试用化学方程式和简要文字表达其理由。____________________ |