已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625kJ·g-1。下列热化学方程式中不正确的是( )
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H =-890kJ/mol |
B.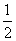 CH4(g)+O2(g)= CH4(g)+O2(g)=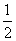 CO2(g)+H2O(l);△H=-445kJ/mol CO2(g)+H2O(l);△H=-445kJ/mol |
C.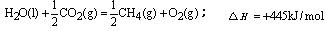 |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-55.625kJ/mol |
下列物质属于弱电解质的是
| A.CH3CH2OH | B.SO2 | C.NH3·H2O | D.HNO3 |
某化合物6.2g在氧气中完全燃烧,只生成8.8gCO2和5.4gH2O.下列说法正确的是
| A.该化合物仅含碳、氢两种元素 |
| B.该化合物中碳、氢原子个教比为1:2 |
| C.无法确定该化合物是否含有氧元素 |
| D.该化合物中一定含有氧元素 |
下列液体分别和溴水混合并振荡,静置后分为两层,水层、油层均为无色的是
| A.辛烷 | B.戊炔 | C.CCl4 | D.NaOH溶液 |
将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水,对于气体烃的组成判断正确的是
| A.一定有甲烷 | B.一定有乙烯 | C.一定没有甲烷 | D.一定没有乙稀 |
1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)
| A.乙炔 | B.丙炔 | C.丁炔 | D.丁二烯 |