聚四氟乙烯的耐热性和化学稳定性都超过了其他合成材料,号称“塑料王”。在工业生产上有广泛的应用,其合成路线如下: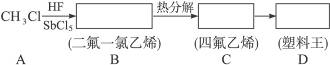
试完成下列各题:
(1)在直方框内填写有机物的结构简式。
(2)写出下列反应的化学方程式:
B→C:__________________________________________________________________;
C→D:__________________________________________________________________。
下图表示NH4NO3和D物质为初始反应物发生的一系列变化,其中,在常温下B为液态,F为不溶于水但可溶于酸的白色固体,G与I为无色气体,G能使湿润的红色石蕊试纸变蓝。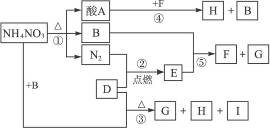
(1)D和H的化学式:D_____________,H_____________,G与E的电子式:G_____________, E_____________。
(2)写出下列反应的方程式:反应①_____________;反应②_____________。
氮可以形成多种离子,如N3-、 、
、 、
、 、
、 、
、 等,已知
等,已知 与
与 是由中性分子结合质子形成的,有类似于
是由中性分子结合质子形成的,有类似于 的性质,另外氮与氢也能形成NH3、N2H4、N3H5、N4H6、N5H7……
的性质,另外氮与氢也能形成NH3、N2H4、N3H5、N4H6、N5H7……
(1)一个 含有__________________________个电子,
含有__________________________个电子, 的电子式为____________。
的电子式为____________。
(2)形成 的中性分子的结构式是_____________________。
的中性分子的结构式是_____________________。
(3) 在强碱溶液中反应的离子方程式:_____________________________。
在强碱溶液中反应的离子方程式:_____________________________。
(4)NH3、N2H4、N3H5、N4H6、N5H7是否互为同系物,为什么?__________________________。
(5)写出N5H7可能的结构简式______________________________。
(6)这一系列化合物中N的质量分数最大值应小于____________%。
在一定条件下,某元素的氢化物X可完全分解为两种单质Y和Z。若已知:
①反应前的X与反应后生成的Z的物质的量之比n(X)∶n(Z)=2∶3。
②单质Y的分子为正四面体构型。
请填写下列空白。
(1)单质Y是______________,单质Z是_________________(填写名称或化学式)。
(2)Y分子中共含________________个共价键。
(3)X分解为Y和Z的化学方程式为:____________________________________。
下图是A→E五种含氮物质的相互转化关系图。其中A、B、C、D常温下都是气体,B为红棕色,写出A、B、C、D、E的化学式和各步反应的化学方程式。
(1)各物质的化学式:
A.____________,B.____________,C.____________,D.____________,E.____________。
(2)各步反应的方程式为:
①____________________________________________________________________________。
②____________________________________________________________________________。
③____________________________________________________________________________。
④____________________________________________________________________________。
有A、B、C、D、E五种主族元素,原子序数依次增大,且不超过36。已知B、C、D同周期,A与D同主族,C与E同主族。A原子最外层电子数为内层电子数的3倍,C原子的内层电子总数为最外层电子数的2倍,B在同周期主族元素中原子半径最大。
(1)写出B2A2的电子式:______________________________________________________。
(2)已知E2A3为有剧毒的白色固体,微溶于水,易溶于浓HCl和NaOH溶液。写出E2A3分别和浓HCl和NaOH溶液反应的化学方程式:
E2A3与浓HCl反应:______________________________________________________________
E2A3与NaOH溶液反应:___________________________________________________________
(3)取E2A3的HCl溶液,通入D的氢化物,发生复分解反应,析出一种黄色沉淀,其反应的化学方程式为:______________________________________________________________。