有四种无色液体:60%的酒精、福尔马林、甲酸和醋酸。只使用一种试剂M鉴别它们,其鉴别过程如下: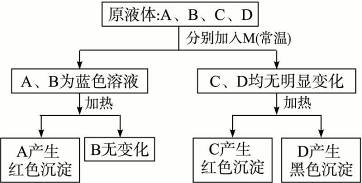
(1)试填写A—D所含有机物的结构简式。
A:______________,B:_______________,C:_______________,D:______________。
(2)试剂M的化学式:______________________________。
用A+、B-、C2―、D、E、F、G分别表示含有18个电子的7种微粒(离子或分子),请回答:
(1)A元素是、B元素是、C元素是(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其单质在常温下呈浅黄绿色,分子式是。
(4)F是由两种元素组成的三原子分子,其结构式是。
(5)G分子中含有4个原子,其分子式是。
下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
请回答下列问题:
(1)B的化学式为____________。
(2)H的电子式为____________。
(3)写出反应③的离子方程式 。
(4)写出反应④的化学方程式 。
(15分)(1)下列为生活中常用药品:
A.碘酒 B.青霉素 C.阿司匹林
D.葡萄糖注射液 E.抗酸药(主要成分为碳酸氢钠)
①上述药品中属于抗生素的是__________。(填字母,下同)
②能为人体直接提供能量的是__________。
③下列关于药物使用的说法中,正确的是________。
A.碘酒能使蛋白质变性,常用于外敷消毒
B.长期大量服用阿司匹林可预防疾病,没有毒副作用
C.使用青霉素,可直接静脉注射,不需进行皮肤敏感试验
D.随着平价药房的开设,生病了都可以到药店自己买药服用,不用到医院就诊
④碳酸氢钠可防治胃酸分泌过多,其发挥功效时的离子方程式为_________________。
(2)(5分)材料与社会生活密不可分。
①在下列材料中,属于无机非金属材料的是________(填字母)。
A.硬币 B.聚氯乙烯塑料 C.氮化硅陶瓷
②钢铁的生产与使用是人类文明和生活进步的一个重要标志。
工业炼铁的主要化学反应方程式为 。
③炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。试回答:铁锅的腐蚀主要是由________腐蚀造成的。为防止轮船的船体在海水中被腐蚀,一般在船身连接________(填“锌块”或“铜块”)。
(3)(6分)保持洁净安全的生存环境已成为全人类的共识。
①下列措施不利于改善环境质量的是________(填字母)。
A.在燃煤中添加石灰石粉末以减少酸雨的发生
B.为实现“低碳世博”,上海世博会很多展馆采用光电转化装置
C.对所有垃圾通过露天焚烧或深埋的方式进行处理
D.利用二氧化碳等原料合成聚碳酸酯类可降解塑料代替聚乙烯
②对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为 。
③居室装修所使用的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是。
④获得洁净安全的饮用水是每个人的正常需要。
对饮用水常使用漂白粉或漂白精片进行杀菌消毒,漂白粉的有效成分为________。加入明矾起净水作用,写出Al3+水解的离子方程式: 。
(本题共14分)A、B、C、D 四种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称:;B在周期表中的位置第周期,第族;
(2)A、B形成的化合物为化合物;(A.离子B.共价)
(3)C的元素符号:,C的最高价氧化物的化学式:;
(4) D的最高价氧化物对应的水化物的化学式:。
(本题共10分) A、B、C、D 四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。则元素:A为B为C为,D的质子数和中子数相等,D 的原子符号为:,它的最高价氧化物对应的水化物:。