在下列两个反应中被氧化的氯元素与被还原的氯元素的质量之比各为多少?
(1)2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O
(2)3Cl2+6KOH 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
从铝土矿(主要成分是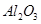 ,含
,含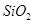 、
、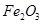 、MgO等杂质)中提取Al2O3的两种工艺品流程如下:
、MgO等杂质)中提取Al2O3的两种工艺品流程如下: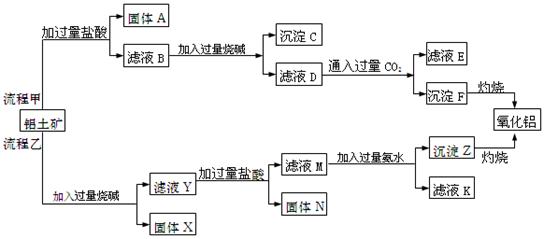
请回答下列问题:
(1)写出相应物质的的化学式:固体A,固体N,
滤液D中溶质为。
(2)流程甲加入盐酸后生成Al3+的离子方程式为。
(3)流程乙加入烧碱后生成水玻璃溶液的化学方程式为。
某金属A及其化合物之间有如下的转化关系: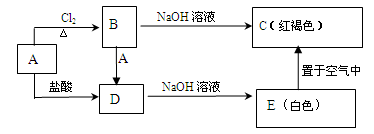
试回答下列问题:
(1)D的溶液与NaOH 溶液混合后的现象是
。
(2)反应B转化成D的离子方程式是。
(3)把B溶液滴入沸水中可以得到红褐色的液体,用一束光通过该液体产生。
(6分)氯水中含有多种成分,因而具有多重性质,根据氯水分别与如图四种物质发生的反应,填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
(1)能证明氯水具有漂白性的是__________(填“a”、“b”、“c”或“d”)。
(2)C过程中的现象是_______________________,b过程中的离子方程式为______________________。
(3)a过程中的化学方程式为_____________________________。
氯酸钾与浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,反应的化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O↑
(1)用双线桥表示上述反应中电子转移的方向和数目。
(2)浓盐酸在该反应中表现的性质是_______________(填序号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)上述反应产生0.1molCl2时,转移的电子数为_____________。
(6分)如图A、B、C、D、E各代表铁、水、三氧化硫、盐酸和氢氧化钡中的一种物质。在常温下,相连环物质之间能发生反应,不相连环物质之间不能发生反应。且B的相对分子质量小于D。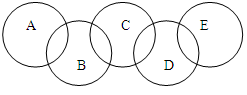
(1)五中物质中属于氧化物的有(填化学式)。
(2)请写出氢氧化钡的电离方程式。
(3)请写出铁与水蒸汽在高温下发生反应的化学方程式
。
(4)请写出下列物质的化学式:B,D(填化学式)。