节能减排是当今社会的热门话题,研发混合动力汽车对于中国汽车业的未来具有重要的战略意义。混合动力汽车持续工作时间长,动力性好的优点,无污染、低噪声的好处,汽车的热效率可提高10%以上,废气排放可改善30%以上,某种混合动力汽车的动力系统由“1.6L汽油机十自动变速器十20kW十200V镍氢电池”组成。
①混合动力汽车所用的燃料之一是乙醇,lg乙醇完全燃烧生成CO2气体和液态H2O放出30.0kJ热量,写出乙醇燃烧的燃烧热的热化学方程式 。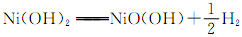 ②镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充电时发生反应 。其放电时的正极的电极反应方程式为 。
②镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充电时发生反应 。其放电时的正极的电极反应方程式为 。
③常温下,同浓度的Na2CO3溶液和NaHCO3溶液的pH都大于7,两者中哪种的pH更大,其原因是 。0.1mol·L-1 Na2CO3中阴离子浓度大小关系是 ,向0.1mol·L-1 NaHCO3溶液中滴入少量氢氧化钡溶液,则发生反应的离子方程式为: 。
(2)二氧化锰、锌是制备干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)
联合生产二氧化锰、锌的工艺如下: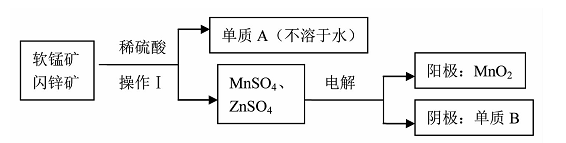
①操作Ⅰ需要的玻璃仪器是 。
②软锰矿(含MnO2)和闪锌矿与硫酸反应的化学方程式为 ,上述电解过程中,当阴极生成6.5g B时阳极生成的MnO2的质量为 。
③利用铝热反应原理,可以从软锰矿中提取锰,发生的化学方程式为 。
[化学---选修5:有机化学基础]
已知: (-R表示烃基)
(-R表示烃基) 苯甲醇+苯甲酸钾
苯甲醇+苯甲酸钾
可由下列反应路线合成结晶玫瑰(只列出部分反应条件)
(1)A是苯的一种同系物,相同条件下,其蒸气对氢气的相对密度是46,则A的名称是。
(2)C中的官能团是_____________。
(3)反应③的化学方程式为____________________。
(4)经反应路线④得到的副产物加水萃取、分液,能除去的副产物是。
(5)已知: ,则经反应路线⑤得到一种副产物,其核磁共振氢谱有4种峰,各组吸收峰的面积之比为。
,则经反应路线⑤得到一种副产物,其核磁共振氢谱有4种峰,各组吸收峰的面积之比为。
(6)G的同分异构体L遇FeCl3溶液显色,与足量饱和溴水反应未见白色沉淀产生,则L与NaOH的乙醇溶液共热,所得有机物的结构简式为(只写一种)。
(7)⑥的化学方程式是。
(8)C有多种同分异构体,其中属于芳香族化合物的有种(不包括C)。
[化学——选修3:物质结构与性质]已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;B的最外层电子数为其内层电子数的3倍;A与C可形成离子化合物C3A2;D是地壳中含量最多的金属元素;E原子核外的M层中有两对成对电子;F原子核外最外层只有1个电子,其余各层电子均充满。根据以上信息,回答下列问题:(A、B、C、D、E、F用所对应的元素符号表示)。
(1)F原子的核外电子排布式为,A、B、C、D、E的第一电离能最小的是。
(2)C的氧化物的熔点远高于E的氧化物的熔点,原因是。
(3)比较B、E的氢化物的沸点_________。
(4)A的最高价含氧酸根离子中,其中心原子是杂化,E的低价氧化物的空间构型为。
(5)A、D形成某种化合物的晶胞结构如图1,则其化学式为。
(6)F单质的晶体的晶胞结构如图2。若F原子的半径是r cm,则F单质的密度的计算公式是。(用NA表示阿伏伽德罗常数)
[化学——选修2:化学与技术](15分)重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”。硫化钡是可溶于水的盐。讨论用重晶石矿制硫酸钡,设计流程如下:
(1)写出步骤①的化学反应方程式,该反应产生的气体具有、等用途。
(2)为进行反应②先要分离出硫化钡,采用的方法是。反应前要在溶液中滴入少量Ba(OH)2溶液,其作用是:。
(3)若B物质在该生产过程中可循环使用,则反应③的化学方程式是:。
(4)有人提出反应②产生了有臭鸡蛋气味的有毒气体,可采用改变反应物的方法避免产生该气体,则反应②的化学方程式是:。此时若要B物质还能循环使用,则C为(写化学式)。BaSO4是因为具有、等性质而可用作“钡餐”。
(1)工业上可利用“甲烷蒸气转化法”生产氢气,反应为甲烷和水蒸气在高温和催化剂存在的条件下生成一氧化碳和氢气,有关反应的能量变化如图1:
则该反应的热化学方程式_____________________________________。
(2)已知温度、压强对甲烷平衡含量的影响如图2,请回答:
①图26-2中a、b、c、d四条曲线中的两条代表压强分别为1Mpa、2Mpa时甲烷含量曲线,其中表示1Mpa的是________。
②该反应的平衡常数:600 ℃时________700 ℃(填“>”“<”或“=”)。
③已知:在700 ℃,1 MPa时,1 mol CH4与1 mol H2O在1 L的密闭容器中反应,6min达到平衡(如图3),此时CH4的转化率为________________,该温度下反应的平衡常数为______________(结果保留小数点后一位数字)。
④从图3分析,由第一次平衡到第二次平衡,平衡移动的方向是_____________(填“向正反应方向”或“向逆反应方向”),采取的措施可能是_____________________。
(3)以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造新型燃料电池,放电过程中,溶液中铵根离子浓度逐渐增大。写出该电池的正极反应式:_________________。
氢化阿托醛 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下:
(1)氢化阿托醛被氧化后的含氧官能团的名称是____________.
(2)在合成路线上②③的反应类型分别为②_____________③________________.
(3)反应④发生的条件是_____________________.
(4)由 反应的化学方程式为_______________________________
反应的化学方程式为_______________________________
(5)1mol氢化阿托醛最多可和____mol氢气加成,1mol氢化阿托醛发生银镜反应可生成________molAg.
(6)D与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的结构简式为________.D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有______种.