工业上为了处理含有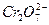 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬的含量已低于排放标准。请回答下列问题:
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬的含量已低于排放标准。请回答下列问题:
(1)两极发生的电极反应式为:阴极:______________;阳极:__________________。
(2)写出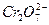 变为Cr3+的离子方程式:__________________________。
变为Cr3+的离子方程式:__________________________。
(3)工业废水由酸性变为碱性的原因是:___________________________。
(4)_________(填“能”或“不能”)改用石墨电极,原因是______________________。
①MgCl2②干冰③冰④Na2O2⑤白磷(P4)⑥硫磺⑦Na2CO3⑧金刚石⑨NaOH ⑩SiO2
(1)以上物质中属于离子晶体的是;
(2)属于分子晶体的是。
(3)属于原子晶体的是_________(填序号)
用电子式表示下列化合物:
H2S:;MgCl2:;NH4Cl:
A、B、C三种有机物,其相对分子质量都小于150,已知B完全燃烧时所消耗的O2和生成的CO2的物质的量相等,C中碳、氢元素总的质量分数为48.39 %。在热的稀硫酸溶液中,1 mol A水解能生成2 mol B和1 mol C。B不能发生银镜反应,但能与NaHCO3溶液反应放出CO2。回答下列问题:
(1)B的分子组成中氢氧原子个数比为;
(2)有机物C的结构简式为;
(3)有机物A的结构简式为;
(4)写出有机物A水解生成B和C的化学方程式。
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。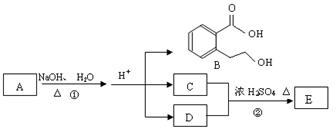
根据上图回答问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为; C分子中的官能团名称是 ______________;化合物B不能发生的反应是(填字母序号):
a.加成反应 b.取代反应 c.消去反应
d.酯化反应 e.水解反应 f.置换反应
(2)反应②的化学方程式是__________________。
(3)A的结构简式是 __________________。
(4)同时符合下列三个条件的B的同分异构体的数目有个。
Ⅰ.含有间二取代苯环结构
Ⅱ.不属于芳香酸形成的酯
Ⅲ.与 FeCl3溶液发生显色反应。
写出其中任意两个同分异构体的结构简式、。
芳香族化合物C10H10O2有如下的转化关系: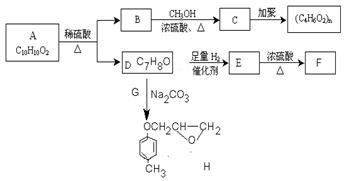
已知F能使Br2/CCl4溶液褪色,且RONa + R’X→ROR’ + NaX
请回答下列问题:
1.写出反应类型。
反应B → C反应 E→F
2.请分别写出A、F的结构简式
AF
3.若有机物M与C互为同分异构体,
则与有机物B互为同系物的M的同分异构体有种。
4. 请写出B→C反应的化学反应方程式
5.请写出D→H反应的化学反应方程式