某有机物结构简式为 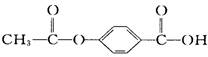 ,1 mol该有机物在合适的条件下与NaOH反应,最多可消耗NaOH的物质的量为 ( )
,1 mol该有机物在合适的条件下与NaOH反应,最多可消耗NaOH的物质的量为 ( )
| A.5 mol |
| B.4 mol |
| C.3 mol |
| D.2 mol |
下列说法正确的是(NA表示阿伏加德罗常数的值) ( )
| A.摩尔是七个基本物理量之一 |
| B.阿伏加德罗常数就是6.02×1023mol-1 |
| C.1mol氢的质量是2 g |
| D.1mol甲烷的质量与NA个甲烷分子的质量之和相等 |
悬浊液、乳浊液、溶液和胶体都是( )
| A.稳定的液体 | B.透明的液体 | C.混合物 | D.化合物 |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A.碱性氧化物氧化铁 FeO | B.酸性氧化物碳酸气 CO |
| C.酸硫酸 H2SO3 | D.盐纯碱 Na2CO3 |
在互联网上用百度搜索“中央电视台每周质量报告”时,可搜索到被曝光的事件中一定涉及到化学变化的是( )
| A.用淀粉、蔗糖、奶香精等掺和成“假奶粉” |
| B.用工业石蜡等给瓜子“美容” |
| C.用墨汁浸泡劣质木耳制作“黑”木耳 |
| D.用硫磺燃烧法熏蒸中药材 |
下列物质属于电解质的是( )
| A.盐酸 | B.石墨 | C.酒精 | D.硫酸钡 |