常温下,将Fe粉和S粉混合,不发生反应。某课外活动小组将Fe粉和S粉按物质的量比1∶1混合均匀,并置于水平放置且隔绝空气的玻璃管中,加热片刻,反应开始,然后撤去酒精灯,发现反应仍能剧烈进行,并使生成的固体呈红热状态。试完成下列问题:
(1)上述现象说明了_____________________________。
(2)将生成的黑色固体置于稀H2SO4中,有气体放出,写出发生反应的离子方程式__________________________________________________________。
(3)已知H2S是一种剧毒、有刺激性气味的气体,试说明实验室制取H2S时应采用的一条安全措施___________________________。
(4)将21.0 g铁粉(过量)和硫粉混合,在隔绝空气情况下加热,将反应后的全部物质装入到足量的稀盐酸中,则生成气体的体积为____________(标准状况)。
(1)火箭残骸中常现红棕色气体,原因为:

当温度升高时,气体颜色变深,则反应为(填“吸热”或“放热”)
反应。
(2)一定温度下,上述反应的焓变为△H。现将1mol N2O4充入一恒压密闭容器中,
下列示意图正确且能说明反应达到平衡状态的是。
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数
(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,
则0~3s内的平均反应速率v(N2O4)=mol·L-1·s-1。
(1)一定条件下,可逆反应:A2(g)+B2(g)  2C(g)达到平衡时,各物质的
2C(g)达到平衡时,各物质的
平衡浓度分别为:c(A2)=0.5 mol·L-1;c(B2)=0.1 mol·L-1;c(C)=1.6 mol·L-1。
若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:
①a、b应满足的关系式是。
②a的取值范围是。
(2)氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,肼(N2H4)可
作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)="===" N2O4 (1) △H1= -19.5kJ·mol-1
②N2H4(1)+O2(g)="===" N2(g)+2H2O(g)△H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式;
有甲、乙、丙三种有机物,其结构简式如下:
已知A、B、C各代表—CH3、—CHO、—OH中的一种,甲、乙、丙互为同分异构体。
(1)将A、B、C代表的基团填在对应的表格内:
| A |
B |
C |
(2)甲、乙、丙按酸性由强至弱排列的顺序为________。
(3)有机物丙和新制的Cu(OH)2悬浊液共热反应的化学方程式为
______________________________________________
呋喃酚是合成农药的重要中间体,其合成路线如下:
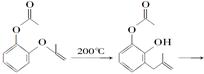

C D E(呋喃酚)
(1)A在空气中久置会由无色转变为棕褐色,其原因是____________________,A在核磁共振氢谱中有____________组峰。
(2)B→C的反应类型是__________________________________。
(3)已知X的分子式为C4H7Cl。写出A→B的化学方程式__________________。
(4)要鉴别化合物C和D,适宜的试是_________________________________。
(5)B的同分异构体很多,符合下列条件的有______种,写出其中能发生银镜反应的同分异构体的结构简式:__________________(任写一种)。
①苯的衍生物 ②有两个互为对位的取代基
③含有酯基
写出下列物质转化的化学方程式,并指出反应类型
(1)溴乙烷 → 乙醇
(2)甲苯 → TNT
(3)乙醇→乙醛
(4)乙醛 +银氨溶液→
(5)氯乙烯→聚氯乙烯