某温度下在密闭容器中发生如下反应2M(g)+N(g) 2E(g),若开始时只充入2molE气体,达平衡时,混合气体的压强比起始增大了20%;若开始时只充入3molM和1molN的混合气体,达到平衡时M的转化率为 ( )
| A.<60% | B.="40%" | C.<40% | D.>60%  |
下列物质中,属于目前世界上用量最大、用途最广的合金是
| A.青铜 | B.钢材 | C.18K金 | D.钛合金 |
蛋白质的下列哪个性质可以用于蛋白质的提纯分离
| A.水解 | B.盐析 | C.变性 | D.颜色反应 |
下列叙述中不正确的是
| A.食盐加碘所添加的是碘酸钾 |
| B.油脂既能为人体提供热量,又能提供人体必需脂肪酸 |
| C.棉花、羊毛及合成纤维完全燃烧都只生成二氧化碳和水 |
| D.蛋白质遇饱和硫酸铵溶液产生的沉淀能重新溶于水 |
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟,应理解为
| A.单质 | B.分子 | C.元素 | D.氧化物 |
人体正常的血红蛋白中应含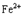 。若误食亚硝酸盐,则导致血红蛋白中
。若误食亚硝酸盐,则导致血红蛋白中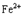 转化为高铁血红蛋白而中毒。服用维生素C可解除亚硝酸盐中毒。下列叙述中正确的是
转化为高铁血红蛋白而中毒。服用维生素C可解除亚硝酸盐中毒。下列叙述中正确的是
| A.亚硝酸盐是还原剂 | B.维生素C是氧化剂 |
C.维生素C将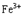 还原为 还原为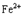 |
D.亚硝酸盐被氧化 |